
����ѧ����ѡ��3�����ʽṹ�����ʡ���15�֣�
���� aA��bB��CC��dD��eE��gG���ֶ����ڷǽ���Ԫ�أ�a+b=c,a+c=d,a+d=e,d+e=g,C��E��G�ĵ��ʈV������ѧ���������ֻ����ͬ�������塣��ش��������⣺
I.��1��G��̬ԭ�ӵĺ�������Ų�ʽΪ ��
��2��C��D��EԪ�صĵ�һ�������ɴ���С�Ĺ�ϵ�� ������Ԫ�ط��ű�ʾ��
��3����Ƚ�C2A4��D2A4��G2A4���ֻ�����ķе��ɸߵ��͵�˳��Ϊ ��
��.BG��һ����ĥ���ϣ���ṹ����ʯ���ƣ���ͼΪ�侧��ṹ��Ԫ��
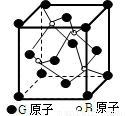
������B�����廯���G�����廯���ڸ������������ķ�Χ�кϳ�
��1��ָ��B�����廯����B���ӻ���ʽΪ ��G�����廯����ӵĽṹΪ �͡�
��2��д���ϳ�BG�Ļ�ѧ����ʽΪ ��
��3����֪������B��Gԭ�ӵ��������Ϊapm,��þ�����ܶȵı���ʽΪ g/cm3��
I.��1��[Ne]3s23p3 �� 1s22s22p63s23p6(2��) ��2��N>O>C(2��) ��3��N2H4>P2H4>C2H4(2��)
�� (1)sp2 ��2�֣� ���� ��2�֣� ��2��BBr3+PBr3+3H2 BP+6HBr(2��)
BP+6HBr(2��)
��3�� ��3�֣�
��3�֣�
��������
�������������aA��bB��CC��dD��eE��gG���ֶ����ڷǽ���Ԫ�أ�a+b=c,a+c=d,a+d=e,d+e=g,C��E��G�ĵ��ʈV������ѧ���������ֻ����ͬ�������壬��Ӧ����̼Ԫ�ء���Ԫ�غ���Ԫ�أ�����A��H��B��B��C��C��D��N��e��O��G��P��
I.��1��P��ԭ��������15������ݺ�������Ų���֪P��̬ԭ�ӵĺ�������Ų�ʽΪ[Ne]3s23p3 �� 1s22s22p63s23p6(��
��2���ǽ�����Խǿ�����һ������Խ�����ڵ�Ԫ�ص�2p������Ӵ��ڰ����״̬�ȶ���ǿ����˵�Ԫ�صĵ�һ�����ܴ�����Ԫ�صĵ�һ�����ܣ���C��D��EԪ�صĵ�һ�������ɴ���С�Ĺ�ϵ��N>O>C��
��3����Ԫ�طǽ�����ǿ�����N2H4���Ӽ����������е���ߡ�P2H4��C2H4���Ƿ��Ӿ��壬����Ӽ�������Խ��е���ߡ����Ӽ�����������Է������������ȣ���C2A4��D2A4��G2A4���ֻ�����ķе��ɸߵ��͵�˳��ΪN2H4>P2H4>C2H4��
��.BG��һ����ĥ���ϣ���ṹ����ʯ���ƣ���ͼΪ�侧��ṹ��Ԫ��
������B�����廯���G�����廯���ڸ������������ķ�Χ�кϳ�
��1��B�����廯����BBr3��Bû�й¶Ե��ӣ��۲���Ӷ�����3������ƽ�������νṹ����B���ӻ���ʽΪsp2��G�����廯��PBr3������Pԭ�Ӻ��У�5��1��3����2��1�Թ¶Ե��ӣ��۲���Ӷ�����4������ӵĽṹΪ�����Ρ�
��2��BG����B�����廯���G�����廯���ڸ������������ķ�Χ�кϳɣ���Ӧ�Ļ�ѧ����ʽΪBBr3+PBr3+3H2 BP+6HBr��
BP+6HBr��
��3����֪������B��Gԭ�ӵ��������Ϊapm�������������Խ�����4a��10��10cm������������ı߳���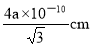 �����ݾ����ṹ��֪�����к���4��BP����
�����ݾ����ṹ��֪�����к���4��BP���� ,��þ�����ܶȵ�
,��þ�����ܶȵ� g/cm3��
g/cm3��
���㣺�������ʽṹ������ģ�������Ӧ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ĵ�ʡ�����и����ڶ�������Կ������ۻ�ѧ�Ծ��������棩 ���ͣ������
��14�֣������������ų������ı������Ҫ��BaCO3��BaSO3��Ba(FeO2)2�ȣݣ�ij��Ҫ����BaCO3�Ļ��������ñ�����ȡBa(NO3)2���弰����������䲿�ֹ����������£�

��֪��i Fe(OH)3��Fe(OH)2��ȫ����ʱ����Һ��pH�ֱ�Ϊ3.2��9.7��
ii Ba(NO3)2����ˮ���ܽ�Ƚϴ�����ˮ���ܽ�Ƚ�С��
iii KSP(BaSO4)��1.1��10-10��KSP(BaCO3)=5.1��10-9��
��1���ó�������BaCO3��������BaSO4���������ᴿ�ķ����ǣ�����Ʒ���������ı���Na2CO3��Һ�У���ֽ��裬���ˣ�ϴ�ӡ������ӷ���ʽ�ͱ�Ҫ������˵���ᴿԭ���� ��
��2��������������ʱ��Ba(FeO2)2��HNO3��Ӧ�������������Σ���ѧ����ʽΪ�� ��
��3���ó���ϱ���ʵ�ʣ�ѡ�õ�XΪ ��������ѡ����ѡ������2Ϊ ��д����ѧʽ����
�� BaCl2 ��Ba(NO3)2 ��BaCO3 �� Ba(OH)2
��4������3���ĸҺӦѭ�������� �С����a������b����c����
��5����ȡw g������������ˮ���������������ᣬ��ַ�Ӧ���ˡ�ϴ�ӡ����������������Ϊm g�����Ba(NO3)2�Ĵ���Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ϻ��о�����������ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���õ��ԭ��������Ƥ�����һ��п���й�������ȷ����
A����Ϊ������пΪ���� B����Ϊ������пΪ����
C���ÿ��������������Һ D��пԪ�ؼȱ������ֱ���ԭ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������ʡ�����и�����ѧ�ڵڶ��ν�ѧ�������л�ѧ�Ծ��������棩 ���ͣ�ѡ����
700��ʱ�����ݻ������1L�ܱ������г���һ������CO��H2O��������Ӧ��
CO(g)+ H2O(g) CO2(g)+H2(g����Ӧ�����вⶨ�IJ������ݼ��±�������t1<t2��
CO2(g)+H2(g����Ӧ�����вⶨ�IJ������ݼ��±�������t1<t2��

����˵������ȷ����
A��O��t1 min��ƽ����Ӧ����Ϊv��H2��=  mol��L��l��min��1
mol��L��l��min��1
B�����������������䣬�������ڵ�ѹǿ���ı�ʱ���÷�Ӧһ���ﵽ�˻�ѧƽ��״̬
C�����������������䣬����ʼʱ�������г���0.60mol CO��1.20mol H2O����ﵽƽ��ʱn��CO2��=0.40mol
D�����������������䣬��ƽ����ϵ����ͨ��0.20mol H2O����ԭƽ����ȣ��ﵽ��ƽ��ʱCO��ת��������CO2��Ũ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������ʡ�����и�����ѧ�ڵڶ��ν�ѧ�������л�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʵ��������ܴﵽԤ��Ŀ�ĵ���
A���ñ���NaHCO3��Һ��ȥCO2��������HCl
B��NH4C1��I2�Ĺ�����������ü��ȵķ�������
C��ֲ���ͺ�ˮ�Ļ��������÷�Һ�ķ�������
D����ˮ�е��嵥�ʿ��������Ȼ�̼��ȡ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ�����и���1�¿�ǰ��Ӧ��ѵ�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
���������������
A���ڼ��Ƚ��������¼���MgO���ɳ�ȥMgCl2��Һ�е�Fe3��
B��pH=4.5�ķ���֭��c(H�� )��pH=6.5��ţ����c(H��)��100��
C�������£�CH3COONa��CH3COOH�Ļ����Һ��(pH=7):C(Na��)=c(CH3COO�D)>c(CH3COOH)>c(H��)=c(OH�D)
D.�����£�Cd(OH)2��Co(OH)2�Ļ������Һ�У�c(Cd@+)��c(Co)��3.5������֪��KSP(Cd(OH)2)=7.2��10-15, KSP(Co(OH)2)=1.8��10-15
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ�����и���12���¿����ۻ�ѧ�Ծ��������棩 ���ͣ������
��18�֣���ͼ��ʾ�Ļ�����������Ϊ���������飬������������Ʊ�ҩ��ͺϳɸ߷��Ӳ��ϡ�
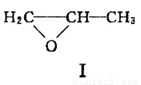
��1���������ķ���ʽΪ______________��
��2����������ڴ�������������ˮ������Ӧ�õ���Ԫ�����÷�Ӧ�Ļ�ѧ����ʽΪ__________________��
��3����������һ����������ʧ����ҩ����ĺϳ�·�����£�
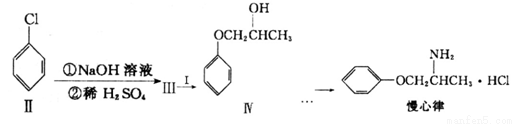
�٢�+������ķ�Ӧ����Ϊ________����Ľṹ��ʽΪ_________________��
��д�����������Ũ��ˮ��Ӧ�Ļ�ѧ����ʽ��______________________��
���ɢ�͢��Ʊ����Ĺ�����������������V���ɣ�V�����Ϊͬ���칹�壬V�Ľṹ��ʽΪ_______________��
��4����֪��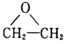 +CH3COOH��
+CH3COOH�� �ۺ���
�ۺ���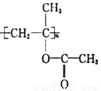 �������Ʊ�����ˮ����֬���䵥��Ľṹ��ʽΪ__________________����CH3COOH�ͻ�����IΪԭ�Ͽɺϳɸõ��壬�漰�ķ�Ӧ�Ļ�ѧ����ʽΪ____________��_____________��
�������Ʊ�����ˮ����֬���䵥��Ľṹ��ʽΪ__________________����CH3COOH�ͻ�����IΪԭ�Ͽɺϳɸõ��壬�漰�ķ�Ӧ�Ļ�ѧ����ʽΪ____________��_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�γ��и߶�12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
14����ˮD2O�����ӻ�Ϊ1.6��10-15��������PHһ���Ķ������涨PD= ��lgc(D+),���¹���PD��������ȷ����
A��������Һ��PD=7
B����1LD2O����Һ���ܽ�0.01mol NaOD������Һ�����Ϊ1L��������PD=12
C����1L D2O���ܽ� 0.01mol DCl(����Һ�����Ϊ1L)������PD=2
D����100mL 0.25mol��L-1��NaOD��ˮ��Һ�м���50mL 0.2mol��L-1DCl�ĵ���ˮ��Һ������PD=1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ĵ�ʡ�㰲�и�����һ����ۻ�ѧ�Ծ��������棩 ���ͣ������
(14��)��ij�¶��¡��ݻ���Ϊ2L�������ܱ������У�����ͬ��ʽͶ�뷴Ӧ����ֺ��º��ݣ�ʹ֮������Ӧ��2 H2��g����CO��g�� CH3OH��g����
CH3OH��g����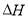 ����a KJ��mol��1(a>0)����ʼͶ����������ﵽƽ��ʱ���й��������£�
����a KJ��mol��1(a>0)����ʼͶ����������ﵽƽ��ʱ���й��������£�
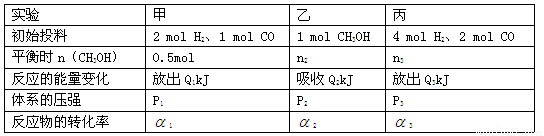
��1�����¶��´˷�Ӧ��Ӧ����ܼ��ܺ� ������ڡ������ڡ���С�ڡ�����������ܼ��ܺ͡�
��2���ڸ��¶��£�����������ӷ�Ӧ��ʼ��ƽ������ʱ��Ϊ4 min����H2��ƽ����Ӧ����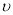 ( H2)Ϊ ��
( H2)Ϊ ��
��3������ѡ����˵���������еķ�Ӧ�Ѿ��ﵽƽ��״̬���� ������ţ���
A��������H2��CO��CH3OH�����ʵ���֮��Ϊ2��1��1
B��������������ܶȱ��ֺ㶨
C��������H2���������������ֺ㶨
D��2V����H2��=V�棨CO��
��4���������У�ƽ����������ݻ�ѹ����ԭ����l/2�������������䣬��ƽ����ϵ������Ӱ����
������ĸ��ţ���
A��c(H2)����
B������Ӧ���ʼӿ죬�淴Ӧ���ʼ���
C��CH3OH �����ʵ�������
D������ƽ��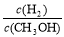 ��С
��С
E��ƽ�ⳣ��K����
��5�����������еķ�Ӧ�ֱ��ƽ��ʱ�������ݹ�ϵ��ȷ���� ������ţ���
A��Q1��Q2��a B����3����1
C��P3��2P1��2P2 D��n2��n3��1.0mol
��6����֪����3CO(g) +3H2(g) CH3OCH3(g) +CO2(g) ��H=��247kJ��mol��l
CH3OCH3(g) +CO2(g) ��H=��247kJ��mol��l
��2CH3OH(g) CH3OCH3(g)+H2O(g) ��H= ��24 kJ��mol��l
CH3OCH3(g)+H2O(g) ��H= ��24 kJ��mol��l
��CO(g)+H2O(g) CO2(g)+H2(g) ��H= ��41 kJ��mol��l
CO2(g)+H2(g) ��H= ��41 kJ��mol��l
2 H2��g����CO��g�� CH3OH��g����
CH3OH��g����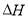 ����a KJ��mol��1 ���� a��
����a KJ��mol��1 ���� a��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com