
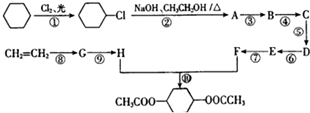
 .反应⑧可以是乙烯与水发生加成反应生成G为CH3CH2OH,G发生氧化反应生成乙酸,或者为乙烯氧化生成乙醛,再发生氧化反应生成乙酸.由合成路线可知,反应①为光照条件下的取代反应,反应②为卤代烃在NaOH/醇条件下的消去反应,则A为
.反应⑧可以是乙烯与水发生加成反应生成G为CH3CH2OH,G发生氧化反应生成乙酸,或者为乙烯氧化生成乙醛,再发生氧化反应生成乙酸.由合成路线可知,反应①为光照条件下的取代反应,反应②为卤代烃在NaOH/醇条件下的消去反应,则A为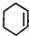 ,A可以与溴发生加成反应生成B为
,A可以与溴发生加成反应生成B为 ,B再发生消去反应生成C为
,B再发生消去反应生成C为 ,C与溴水发生1,4-加成生成D为
,C与溴水发生1,4-加成生成D为 ,D与氢气发生加成反应生成E为
,D与氢气发生加成反应生成E为 ,E发生水解反应生成F,据此解答.
,E发生水解反应生成F,据此解答. .反应⑧可以是乙烯与水发生加成反应生成G为CH3CH2OH,G发生氧化反应生成乙酸,或者为乙烯氧化生成乙醛,再发生氧化反应生成乙酸.由合成路线可知,反应①为光照条件下的取代反应,反应②为卤代烃在NaOH/醇条件下的消去反应,则A为
.反应⑧可以是乙烯与水发生加成反应生成G为CH3CH2OH,G发生氧化反应生成乙酸,或者为乙烯氧化生成乙醛,再发生氧化反应生成乙酸.由合成路线可知,反应①为光照条件下的取代反应,反应②为卤代烃在NaOH/醇条件下的消去反应,则A为 ,A可以与溴发生加成反应生成B为
,A可以与溴发生加成反应生成B为 ,B再发生消去反应生成C为
,B再发生消去反应生成C为 ,C与溴水发生1,4-加成生成D为
,C与溴水发生1,4-加成生成D为 ,D与氢气发生加成反应生成E为
,D与氢气发生加成反应生成E为 ,E发生水解反应生成F,
,E发生水解反应生成F, ,故答案为:
,故答案为: ;
; ,D中所含官能团的名称为:碳碳双键、溴原子,故答案为:碳碳双键、溴原子;
,D中所含官能团的名称为:碳碳双键、溴原子,故答案为:碳碳双键、溴原子; ;
; ,
, ;
; ;
;

 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:
| A、氮的氧化物是汽车尾气中的主要污染物之一 |
| B、氮的氧化物既可形成酸雨,又是光化学污染的主要成分 |
| C、化石燃料的燃烧是造成空气中二氧化硫含量增多的主要因素 |
| D、酸雨在空气中静置一段时间后,雨水的酸性会慢慢减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| ① | ② | ③ | ④ | |
| A | NaCl | Na2SO4 | KCl | Mg(NO3)2 |
| B | Na2SO4 | K2SO4 | KCl | MgCl2 |
| C | NaCl | K2SO4 | KCl | MgCl2 |
| D | Na2SO4 | K2SO4 | KCl | Mg(NO3)2 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
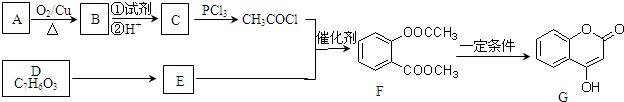
| PCl3 |
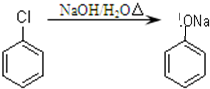 )制取苯酚,而酚羟基一般不易直接与羧酸酯化.苯甲酸苯酚酯(
)制取苯酚,而酚羟基一般不易直接与羧酸酯化.苯甲酸苯酚酯(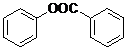 )是一种重要的有机合成中间体.试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任用).
)是一种重要的有机合成中间体.试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任用).| O2 |
| 催化剂 |
| CH3CH2OH |
| 浓H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
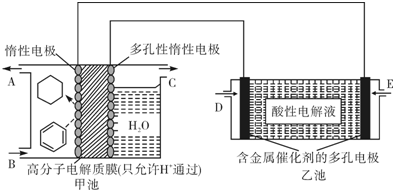
| A、乙池中溶液的pH变大 |
| B、E处通入H2,C处有O2放出 |
| C、甲池中阴极区只有苯被还原 |
| D、导线中共传导11.2mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
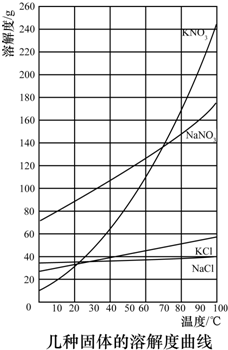
| 2 |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(H+):c(OH-)=1:10-2的溶液中K+、Ba2+、ClO-、CO32-一定能大量存在 | ||
| B、水电离出来的c(H+)=10-13mol/L的溶液中K+、Cl-、NO3-、I-一定能大量存在 | ||
C、往0.1mol/LCH3COOH溶液中通人少量HCl,醋酸的电离平衡向逆反应方向移动,且溶液中
| ||
| D、等物质的量浓度的下列溶液:①H2CO3②Na2CO3③NaHCO3④(NH4)2CO3⑤NH4HCO3中c(CO32-)的大小关系为:②>④>③>⑤>① |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化合物 | 甲 | 乙 | 丙 | 丁 |
| 组成元素 | B、C | A、C | A、D | C、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | Mg(OH)2 | CaCO3 | MgCO3 | Ca(OH)2 | CaSO4 | MgSO4 |
| 溶解度 g/100gH2O | 9.0×10-4 | 1.5×10-3 | 1.0×10-2 | 1.7×10-1 | 2.1×10-1 | 26.7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com