
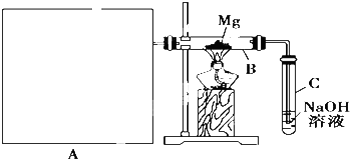
分析 Ⅰ.(1)依据强酸制备弱酸的原理,结和物质的性质,选择实验室制备SO2的试剂;
(2)根据Mg与CO2的反应知Mg与SO2反应能生成氧化镁与单质硫,但单质硫能与镁反应生成硫化镁;二氧化硫有毒,不能直接排放到空气中,可用氢氧化钠吸收过量的二氧化硫;(3)依据反应物状态及反应条件选择合适的发生装置;
(4)该装置中:①A中的水蒸气会进入B与Mg反应,在A、B中间应加干燥装置;②Mg能与SiO2反应,在Mg下方垫一不锈钢片,隔离Mg和SiO2;③尾气处理装置C试管用胶塞封闭,且无防倒吸装置;
Ⅱ.(5)类似于镁和二氧化碳的反应,可生成单质硅和氧化镁;
(6)发现有爆鸣声和火花,说明生成气体,应为SiH4.
解答 解:Ⅰ.(1)制取SO2应用浓H2SO4和亚硫酸盐,选项中不可选用CaSO3,因为CaSO3微溶于水,会附在固体表面,阻碍反应进行,
故答案为:②③;
(2)Mg具有还原性,SO2具有氧化性,两者发生氧化还原反应,反应的方程式为3Mg+SO2$\frac{\underline{\;\;△\;\;}}{\;}$2MgO+MgS(或2Mg+SO2$\frac{\underline{\;\;△\;\;}}{\;}$2MgO+S,Mg+S$\frac{\underline{\;\;△\;\;}}{\;}$MgS),二氧化硫可与碱反应,易防止污染空气,
故答案为:3Mg+SO2$\frac{\underline{\;\;△\;\;}}{\;}$2MgO+MgS(或2Mg+SO2$\frac{\underline{\;\;△\;\;}}{\;}$2MgO+S,Mg+S$\frac{\underline{\;\;△\;\;}}{\;}$MgS);吸收过量二氧化硫,防止污染环境;
(3)实验室制备二氧化硫的反应为固液不加热制取气体的反应,故可用分液漏斗盛80%的H2SO4,用锥形瓶装固体Na2SO3,装置图为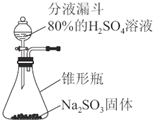 ,
,
故答案为: ;
;
(4)该装置中:①A中的水蒸气会进入B与Mg反应,在A、B中间应加干燥装置;②Mg能与SiO2反应,在Mg下方垫一不锈钢片,隔离Mg和SiO2;③尾气处理装置C试管用胶塞封闭,且无防倒吸装置,
故答案为:在A和B之间没有连接一个干燥装置、C装置未与大气相通、在镁下方未垫一个不锈钢片、镁与玻璃管反应、未设计一个防倒吸装置;
Ⅱ.(5)Mg在点燃的条件下即可与SiO2反应,由题给信息可知类似于镁和二氧化碳的反应,可生成单质硅和氧化镁,反应的方程式为2Mg+SiO2$\frac{\underline{\;\;△\;\;}}{\;}$2MgO+Si,
故答案为:2Mg+SiO2$\frac{\underline{\;\;△\;\;}}{\;}$2MgO+Si;
(6)发现有爆鸣声和火花,说明生成气体,应为SiH4,原因是发生2Mg+Si$\frac{\underline{\;\;△\;\;}}{\;}$Mg2Si,Mg2Si+2H2SO4═2MgSO4+SiH4↑,SiH4+2O2═SiO2+2H2O,金属镁与生成的硅继续反应生成硅化镁,硅化镁与稀硫酸反应生成的SiH4可自燃,
故答案为:金属镁与生成的硅继续反应生成硅化镁,硅化镁与稀硫酸反应生成的SiH4可自燃.
点评 本题为信息题,以镁和二氧化硅的反应为载体考查了二氧化硫的实验室制备及性质检验,侧重培养学生分析问题解决问题的能力,题目难度中等.


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:选择题
| A. | B与A只能组成BA3化合物 | |
| B. | C、D、E形成的化合物与稀硫酸可能发生氧化还原反应 | |
| C. | A、B、C形成的化合物一定不能发生水解 | |
| D. | E的氧化物对应的水化物一定有强的氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能发生脂化反应的酸一定是羧酸 | |
| B. | 蛋白质溶液中加入浓Na2SO4溶液,蛋白质从溶液中凝聚而析出叫盐析 | |
| C. | 天然蛋白质一定条件下水解的最终产物是α-氨基酸 | |
| D. | 淀粉、纤维素和油脂在一定条件下都能发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X、Y、Z在周期表中不可能处于同一周期 | |
| B. | 原子序数Y>X>Z | |
| C. | 简单离子半径:r(X2-)>r(Y+) | |
| D. | Y 单质在X单质中点燃生成物离子个数之比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 鸡屎矾中含有极性共价键 | |
| B. | 铜盐溶液可与铁发生置换反应 | |
| C. | 碱式碳酸铜不稳定,受热易分解 | |
| D. | 鸡屎矾投苦酒中发生的是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| Y | ||||
| Q | W | X | Z |
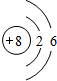 ;举一例说明Z的非金属性比X的非金属性强的事实:酸性强弱;HClO4>H3PO4,或稳定性:HCl>PH3.
;举一例说明Z的非金属性比X的非金属性强的事实:酸性强弱;HClO4>H3PO4,或稳定性:HCl>PH3.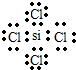 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
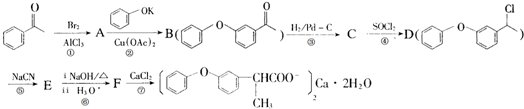
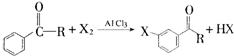
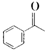 的化学式为C8H8O,该有机物核磁共振氢谱有4种吸收峰,该分子共平面的碳原子至少有7个.
的化学式为C8H8O,该有机物核磁共振氢谱有4种吸收峰,该分子共平面的碳原子至少有7个. 、
、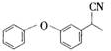 .
.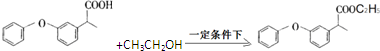 .
.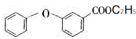 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4.6 g乙醇中含有的C-H键的个数为0.6NA | |
| B. | 34 g H2O2中含有的阴离子数为NA | |
| C. | 标准状况下,V L水含有的氧原子个数约为$\frac{V}{22.4}$NA | |
| D. | 1 mol Fe2+与足量的H2O2溶液反应,转移NA个电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com