
”¾ĢāÄæ”ææĘѧ¼Ņ»ż¼«Ģ½Ė÷ŠĀ¼¼Źõ¶ŌCO2½ųŠŠ×ŪŗĻĄūÓĆ”£
¢ń£®CO2æÉÓĆĄ“ŗĻ³ÉµĶĢ¼Ļ©Ģž£ŗ2CO2(g)+6H2(g)![]() CH2=CH2(g)+4H2O(g) ”÷H=akJ/mol
CH2=CH2(g)+4H2O(g) ”÷H=akJ/mol
Ēė»Ų“š£ŗ
£Ø1£©ŅŃÖŖ£ŗH2ŗĶCH2=CHµÄČ¼ÉÕČČ·Ö±šŹĒ285.8kJ/molŗĶ1411.0kJ/mol£¬ĒŅH2O(g)![]() H2O(£Ø1£©”÷H=-44.0kJ/mol£¬Ōņa=________kJ/mol”£
H2O(£Ø1£©”÷H=-44.0kJ/mol£¬Ōņa=________kJ/mol”£
£Ø2£©ÉĻŹöÓÉCO2ŗĻ³ÉCH2=CH2µÄ·“Ó¦ŌŚ________ĻĀ×Ō·¢½ųŠŠ(Ģī”°øßĪĀ”±»ņ”°µĶĪĀ”±)”£
£Ø3£©ŌŚĢå»żĪŖ1LµÄŗćČŻĆܱÕČŻĘ÷ÖŠ£¬³äČė3molH2ŗĶ1molCO2£¬²āµĆĪĀ¶Č¶ŌCO2µÄĘ½ŗā×Ŗ»ÆĀŹŗĶ“߻ƼĮ“߻Ɗ§ĀŹµÄÓ°ĻģČēĶ¼1ĖłŹ¾”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ________”£

A£®Ę½ŗā³£Źż“󊔣ŗKMN
B£®ĘäĖūĢõ¼ž²»±ä,Čō²»Ź¹ÓĆ“ß»Æ¼Į£¬Ōņ250”ꏱCO2µÄĘ½ŗā×Ŗ»ÆĀŹæÉÄÜĪ»ÓŚµćM1
C£®Ķ¼1ÖŠMµćŹ±,ŅŅĻ©µÄĢå»ż·ÖŹżĪŖ7.7%
D£®µ±Ń¹Ēæ»ņn(H2)/n(CO2)²»±äŹ±¾łæÉÖ¤Ć÷»Æѧ·“Ó¦ŅŃ“ļµ½Ę½ŗāדĢ¬
£Ø4£©±£³ÖĪĀ¶Č²»±ä,ŌŚĢå»żĪŖV LµÄŗćČŻČŻĘ÷ÖŠŅŌn(H2)”Ćn(CO2)=3”Ć1µÄĶ¶ĮĻ±Č¼ÓČė·“Ó¦Īļ,t0Ź±“ļµ½»ÆŃ§Ę½ŗā”£ĒėŌŚĶ¼2ÖŠ×÷³öČŻĘ÷ÄŚ»ģŗĻĘųĢåµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæ![]() Ėꏱ¼ä±ä»ÆµÄĶ¼Ļó”£___________
Ėꏱ¼ä±ä»ÆµÄĶ¼Ļó”£___________

¢ņ£®ĄūÓĆ”°Na-CO2”±µē³Ų½«CO2±ä·ĻĪŖ±¦”£ĪŅ¹śæĘŃŠČĖŌ±ŃŠÖĘ³öµÄæɳäµē”°Na-CO2”±µē³Ų,ŅŌÄĘ²ŗĶ¶ą±ŚĢ¼ÄÉĆ×¹Ü(MWCNT)ĪŖµē¼«²ÄĮĻ,×Ü·“Ó¦ĪŖ4Na+3CO2![]() 2Na2CO3+C”£·ÅµēŹ±øƵē³Ų”°ĪüČė”±CO2,Ę乤×÷ŌĄķČēĶ¼3ĖłŹ¾£ŗ
2Na2CO3+C”£·ÅµēŹ±øƵē³Ų”°ĪüČė”±CO2,Ę乤×÷ŌĄķČēĶ¼3ĖłŹ¾£ŗ

£Ø5£©·ÅµēŹ±,Õż¼«µÄµē¼«·“Ó¦Ź½ĪŖ__________________”£
£Ø6£©ČōÉś³ÉµÄNa2CO3ŗĶCČ«²æ³Į»żŌŚÕż¼«±ķĆę£¬µ±×ŖŅĘ0.2mole-Ź±£¬Õż¼«Ōö¼ÓµÄÖŹĮæĪŖ_______g”£
£Ø7£©Ń”ÓĆøßĀČĖįÄĘĖÄøŹ“¼¶ž¼×ĆŃ×öµē½āŅŗµÄÓŵćŹĒ_____________________”£
”¾“š°ø”æ -127.8 µĶĪĀ C  ”¾×÷Ķ¼ŅŖĒó£ŗOµć×ų±ź(0,12.5)£¬t0Ę½ŗāŹ±
”¾×÷Ķ¼ŅŖĒó£ŗOµć×ų±ź(0,12.5)£¬t0Ę½ŗāŹ±![]() ŌŚ12.5µ½20Ö®¼ä”£”æ 3CO2+4Na++4e-=2Na2CO3+C 11.2 µ¼µēŠŌŗĆ”¢Óė½šŹōÄĘ²»·“Ó¦”¢Äѻӷ¢µČĢŲµć
ŌŚ12.5µ½20Ö®¼ä”£”æ 3CO2+4Na++4e-=2Na2CO3+C 11.2 µ¼µēŠŌŗĆ”¢Óė½šŹōÄĘ²»·“Ó¦”¢Äѻӷ¢µČĢŲµć
”¾½āĪö”æI.(1). ¢Ł H2(g)+1/2O2(g)=H2O(l) ”÷H=285.8kJ/mol£»
¢Ś C2H4(g)+3O2(g)=2H2O(l)+2CO2(g) ”÷H=1411.0kJ/mol£»
¢Ū H2O(g)ØTH2O(l) ”÷H=44kJ/mol
øł¾ŻøĒĖ¹¶ØĀÉ£ŗ6”Į¢Ł¢Ś4”Į¢ŪµĆ2CO2(g)+6H2(g)![]() CH2=CH2(g)+4H2O(g) ”÷H=6”Į(285.8kJ/mol)(1411.0kJ/mol)4”Į(44kJ/mol)= 127.8kJ/mol£¬¹Ź“š°øĪŖ£ŗ127.8£»
CH2=CH2(g)+4H2O(g) ”÷H=6”Į(285.8kJ/mol)(1411.0kJ/mol)4”Į(44kJ/mol)= 127.8kJ/mol£¬¹Ź“š°øĪŖ£ŗ127.8£»
(2). øł¾ŻÉĻĆęĖłµĆČČ»Æѧ·½³ĢŹ½æÉÖŖ£¬”÷H<0¼“ÕżĻņĪŖ·ÅČČ·“Ó¦£¬2CO2(g)+6H2(g)![]() CH2=CH2(g)+4H2O(g)·“Ó¦Ē°ŗóĘųĢåĢå»ż¼õŠ”£¬ģŲ±ä”÷S<0£¬ŅŖĀś×ć”÷HT”÷S<0£¬Ó¦ŌŚµĶĪĀĻĀÄÜ×Ō·¢½ųŠŠ£¬¹Ź“š°øĪŖ£ŗµĶĪĀ£»
CH2=CH2(g)+4H2O(g)·“Ó¦Ē°ŗóĘųĢåĢå»ż¼õŠ”£¬ģŲ±ä”÷S<0£¬ŅŖĀś×ć”÷HT”÷S<0£¬Ó¦ŌŚµĶĪĀĻĀÄÜ×Ō·¢½ųŠŠ£¬¹Ź“š°øĪŖ£ŗµĶĪĀ£»
(3). A. ÉżøßĪĀ¶Č¶žŃõ»ÆĢ¼µÄĘ½ŗā×Ŗ»ÆĀŹ½µµĶ£¬ŌņÉżĪĀĘ½ŗāÄęĻņŅĘ¶Æ£¬ĖłŅŌMµć»ÆŃ§Ę½ŗā³£Źż“óÓŚNµć£¬¹ŹA“ķĪó£»B. “߻ƼĮ²»ÄÜŹ¹Ę½ŗā·¢ÉśŅĘ¶Æ£¬ÓÉĶ¼ĻóæÉÖŖ£¬ĘäĖūĢõ¼ž²»±ä£¬Čō²»Ź¹ÓĆ“ß»Æ¼Į£¬Ōņ250”ꏱCO2µÄĘ½ŗā×Ŗ»ÆĀŹĪ»ÓŚµćM£¬¹ŹB“ķĪó£»C. ŌŚĢå»żĪŖ1LµÄŗćČŻĆܱÕČŻĘ÷ÖŠ£¬³äČė3mollH2ŗĶ1molCO2£¬Ķ¼ÖŠMµćŹ±¶žŃõ»ÆĢ¼×Ŗ»ÆĀŹĪŖ50%£¬
6H2(g)+2CO2(g) ![]() CH2=CH2 (g)+4H2O(g)
CH2=CH2 (g)+4H2O(g)
ĘšŹ¼Įæ(mol) 3 1 0 0
±ä»ÆĮæ(mol) 1.5 0.5 0.25 1
Ę½ŗāĮæ(mol) 1.5 0.5 0.25 1
²śĪļCH2=CH2µÄĢå»ż·ÖŹż=![]() ”Į100%=7.7%£¬¹ŹCÕżČ·£»D£®ÓÉ·½³ĢŹ½æÉÖŖ£¬µ±Ń¹Ēæ²»±äŹ±£¬ĖµĆ÷·“Ó¦“ļµ½ĮĖĘ½ŗāדĢ¬£»ŅņH2ŗĶCO2µÄĘšŹ¼¼ÓČėĮæµČÓŚ»Æѧ¼ĘĮæŹżÖ®±Č£¬Ōņ·“Ó¦¹ż³ĢÖŠn( H2)/n(CO2 )Ź¼ÖÕ²»±ä£¬ĖłŅŌn( H2)/n(CO2 )²»±ä²»ÄÜÖ¤Ć÷»Æѧ·“Ó¦ŅŃ“ļµ½Ę½ŗāדĢ¬£¬¹ŹD“ķĪ󣻓š°øŃ”C£»
”Į100%=7.7%£¬¹ŹCÕżČ·£»D£®ÓÉ·½³ĢŹ½æÉÖŖ£¬µ±Ń¹Ēæ²»±äŹ±£¬ĖµĆ÷·“Ó¦“ļµ½ĮĖĘ½ŗāדĢ¬£»ŅņH2ŗĶCO2µÄĘšŹ¼¼ÓČėĮæµČÓŚ»Æѧ¼ĘĮæŹżÖ®±Č£¬Ōņ·“Ó¦¹ż³ĢÖŠn( H2)/n(CO2 )Ź¼ÖÕ²»±ä£¬ĖłŅŌn( H2)/n(CO2 )²»±ä²»ÄÜÖ¤Ć÷»Æѧ·“Ó¦ŅŃ“ļµ½Ę½ŗāדĢ¬£¬¹ŹD“ķĪ󣻓š°øŃ”C£»
(4).·“Ó¦Ē°»ģŗĻĘųĢåµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæ=![]() =12.5£¬ĖłŅŌĘšµć×ų±źĪŖ(0£¬12.5)£¬Ėę×Å·“Ó¦½ųŠŠ£¬ĘųĢåµÄĪļÖŹµÄĮæ¼õŠ”£¬»ģŗĻĘųĢåµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæŌö“ó£¬ÖĮt0Ź±“ļµ½»ÆŃ§Ę½ŗā£¬ČōČ«²æ×Ŗ»ÆĪŖCH2=CH2ŗĶH2OĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæ=
=12.5£¬ĖłŅŌĘšµć×ų±źĪŖ(0£¬12.5)£¬Ėę×Å·“Ó¦½ųŠŠ£¬ĘųĢåµÄĪļÖŹµÄĮæ¼õŠ”£¬»ģŗĻĘųĢåµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæŌö“ó£¬ÖĮt0Ź±“ļµ½»ÆŃ§Ę½ŗā£¬ČōČ«²æ×Ŗ»ÆĪŖCH2=CH2ŗĶH2OĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæ=![]() =20£¬Ōņt0“ļĘ½ŗāŹ±
=20£¬Ōņt0“ļĘ½ŗāŹ±![]() Ó¦ŌŚĒų¼ä12.5µ½20Ö®¼ä£¬ĖłŅŌĶ¼ĻóĪŖ
Ó¦ŌŚĒų¼ä12.5µ½20Ö®¼ä£¬ĖłŅŌĶ¼ĻóĪŖ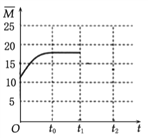 £¬¹Ź“š°øĪŖ£ŗ
£¬¹Ź“š°øĪŖ£ŗ £»
£»
II. (5).ŌŚÕż¼«ÉĻ£¬CO2µĆµē×Ó·¢Éś»¹Ō·“Ó¦£¬¹Źµē¼«·½³ĢŹ½ĪŖ3CO2+4Na++4e-=2Na2CO3+C£¬¹Ź“š°øĪŖ£ŗ3CO2+4Na++4e-=2Na2CO3+C£»
(6).ÓÉÕż¼«·¢ÉśµÄµē¼«·“Ó¦£ŗ3CO2+4Na++4espan>-=2Na2CO3+C
3 4 2 1
0.15 0.2 0.1 0.05
m(×Ü)=m(Na2CO3)+m(C)=106g/mol”Į0.1mol+12g/mol”Į0.05mol=11.2g£¬¹Ź“š°øĪŖ£ŗ11.2£»
(7).Ń”ÓĆó{ĀČĖįÄĘĖÄøŹ“¼¶ž¼×ĆŃ×öµē½āŅŗµÄÓŵćŹĒµ¼µēŠŌŗĆ£¬Óė½šŹōÄĘ²»·“Ó¦£¬Äѻӷ¢µČ£¬¹Ź“š°øĪŖ£ŗµ¼µēŠŌŗĆ”¢Óė½šŹōÄĘ²»·“Ó¦”¢Äѻӷ¢µČÓŠµć”£


 Ņ»ĻßĆūŹ¦ĢįÓÅŹŌ¾ķĻµĮŠ“š°ø
Ņ»ĻßĆūŹ¦ĢįÓÅŹŌ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŌĻĀ±ä»ÆÖŠÖ»ŹĒ¹²¼Ū¼ü±»ĘĘ»µµÄŹĒ
A.ĒāŃõ»ÆÄĘČÜÓŚĖ®B.äåČÜÓŚĖÄĀČ»ÆĢ¼
C.¼×ĶéÓėĀČĘųµÄČ”“ś·“Ó¦D.ĀČ»Æļ§ŹÜČČ·Ö½ā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖA”¢B”¢C”¢D”¢EĪåÖÖŌŖĖŲµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬ĘäÖŠAŌ×ÓĖł“¦µÄÖÜĘŚŹż”¢×åŠņŹż¶¼ÓėĘäŌ×ÓŠņŹżĻąµČ£»BŌ×ÓŗĖĶāµē×ÓÓŠ6ÖÖ²»Ķ¬µÄŌĖ¶ÆדĢ¬£¬s¹ģµĄµē×ÓŹżŹĒp¹ģµĄµē×ÓŹżµÄĮ½±¶£»DŌ×ÓLµē×Ó²ćÉĻÓŠ2¶Ō³É¶Ōµē×Ó£»E+Ō×ÓŗĖĶāÓŠ3²ćµē×ÓĒŅø÷²ć¾ł“¦ÓŚČ«Āś×“Ģ¬£®ĒėĢīŠ“ĻĀĮŠæÕ°×£®
£Ø1£©EŌŖĖŲ»łĢ¬Ō×ÓµÄŗĖĶāµē×ÓÅŲ¼Ź½ĪŖ £®
£Ø2£©B”¢C”¢DČżÖÖŌŖĖŲµÄµŚŅ»µēĄėÄÜŹżÖµÓÉŠ”µ½“óµÄĖ³ŠņĪŖ£ØĢīŌŖĖŲ·ūŗÅ£©£¬ĘäŌŅņĪŖ £®
£Ø3£©B2A4ŹĒÖŲŅŖµÄ»ł±¾ŹÆÓĶ»Æ¹¤ŌĮĻ£®B2A4·Ö×ÓÖŠBŌ×Ó¹ģµĄµÄŌÓ»ÆĄąŠĶĪŖ£»1mol B2A4·Ö×ÓÖŠŗ¬mol¦Ņ¼ü£®
£Ø4£©ŅŃÖŖD”¢EÄÜŠĪ³É¾§°ūČēĶ¼ĖłŹ¾µÄĮ½ÖÖ»ÆŗĻĪļ 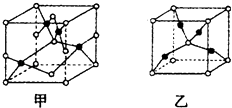 £¬»ÆŗĻĪļµÄ»ÆѧŹ½£¬¼×ĪŖ £¬ ŅŅĪŖ£»øßĪĀŹ±£¬¼×Ņ××Ŗ»ÆĪŖŅŅµÄŌŅņĪŖ £®
£¬»ÆŗĻĪļµÄ»ÆѧŹ½£¬¼×ĪŖ £¬ ŅŅĪŖ£»øßĪĀŹ±£¬¼×Ņ××Ŗ»ÆĪŖŅŅµÄŌŅņĪŖ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æµē½āĮņĖįÄĘČÜŅŗÉś²śĮņĖįŗĶÉÕ¼īČÜŅŗµÄ×°ÖĆČēĶ¼ĖłŹ¾£¬ĘäÖŠŅõ¼«ŗĶŃō¼«¾łĪŖ¶čŠŌµē¼«”£²āµĆĶ¬ĪĀĶ¬Ń¹ĻĀ£¬ĘųĢå¼×ÓėĘųĢåŅŅµÄĢå»ż±ČŌ¼ĪŖl”Ć2£¬ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ£Ø £©
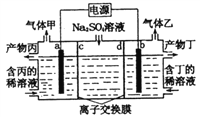
A. aµē¼«·“Ó¦Ź½ĪŖ£ŗ2H++2e-= H2”ü
B. ²śĪļ±ūĪŖĮņĖįČÜŅŗ
C. Ąė×Ó½»»»Ä¤d ĪŖŅõĄė×Ó½»»»Ä¤
D. Ćæ×ŖŅĘ0.1molµē×Ó£¬²śÉś1.12 LµÄĘųĢåŅŅ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ¹ŲÓŚĪļÖŹÖʱøµÄĖµ·Ø“ķĪóµÄŹĒ£Ø £©
A.ĪŅ¹ś¹Å“ś¾ĶŅŃ²ÉÓĆ¼ÓČČµØ·Æ»ņĀĢ·ÆµÄ·½·ØÖĘČ”ĮņĖį
B.µē½āĀČ»ÆĆ¾ČÜŅŗæÉŅŌµĆµ½½šŹōĆ¾
C.ÄĘæÉÓĆÓŚ“ÓīѵÄĀČ»ÆĪļÖŠÖĆ»»³ö½šŹōīŃ
D.¹¤ŅµÉĻŅŌĀČĘųŗĶŹÆ»ŅČéĪŖŌĮĻÖĘŌģĘÆ°×·Ū
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ»ÆѧÄÜŗĶµēÄܵÄĻą»„×Ŗ»Æ£¬ŹĒÄÜĮæ×Ŗ»ÆµÄÖŲŅŖ·½Ź½Ö®Ņ»£¬ČēĶ¼Į½øöŹµŃé×°ÖĆŹĒŹµĻÖ»ÆѧÄÜŗĶµēÄÜĻą»„×Ŗ»ÆµÄ×°ÖĆ£®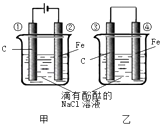
£Ø1£©°Ń»ÆѧÄÜ×Ŗ»ÆĪŖµēÄܵÄ×°ÖĆŹĒ£ØĢī”°¼×”±»ņ”°ŅŅ”±£©
£Ø2£©¢Üµē¼«ÉĻµÄµē¼«·“Ó¦Ź½ĪŖ
£Ø3£©¢Łµē¼«ÉĻµÄµē¼«·“Ó¦Ź½ £¬ ¼ģŃéøƵē¼«·“Ó¦²śĪļµÄ·½·ØŹĒ
£Ø4£©¼×”¢ŅŅĮ½×°ÖƵē¼«ø½½üµÄČÜŅŗŹ×ĻȱäŗģµÄµē¼«·Ö±šŹĒ”¢£ØĢīŠņŗÅ£©
£Ø5£©Š“³ö×°ÖĆ¼×µÄ·“Ó¦×Ü·½³ĢŹ½ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÉčNAĪŖ°¢·ü¼ÓµĀĀŽ³£ŹżÖµ”£ĻĀĮŠÓŠ¹ŲŠšŹöÕżČ·µÄŹĒ
A. 2.4gĆ¾ŌŚ×ćĮæµÄæÕĘųÖŠĶźČ«Č¼ÉÕŹ±ĻūŗÄO2·Ö×ӵďżÄæĪŖ0.1NA
B. 1 molFeČÜÓŚ¹żĮæĻõĖį£¬µē×Ó×ŖŅĘŹżĪŖ3NA
C. 14 gŅŅĻ©ŗĶ±ūĻ©»ģŗĻĘųĢåŗ¬ÓŠĢ¼Ģ¼Ė«¼üŹżÄæĪŖ2NA
D. 5.6L¶žŃõ»ÆĢ¼ĘųĢåÖŠŗ¬ÓŠµÄŃõŌ×ÓŹżĪŖ0.5NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓŠ¹ŲĪļĄķĮæÓėĘ䵄Ī»Ę„ÅäÕżČ·µÄŹĒ£Ø £©
A.ÖŹĮæ©©g
B.·“Ó¦ĖŁĀŹ©©molL©1
C.Ħ¶ūÖŹĮæ©©gmol©1
D.ĘųĢåĦ¶ūĢå»ż©©Lmol©1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”湤ŅµÉĻ£¬Ļņ500”ę×óÓŅµÄĢśŠ¼ÖŠĶØČėCl2Éś²śĪŽĖ®ĀČ»ÆĢś£¬ĘäÖʱø¹ż³ĢÖŠ¾łŅŖČ·±£ĪŽĖ®”£ĻÖÄ£ÄāøĆ¹ż³ĢÓĆĶ¼Ź¾×°ÖĆ½ųŠŠŹµŃé£ŗ

£Ø1£©ŅĒĘ÷aµÄĆū³ĘĪŖ________£¬×°ÖĆAµÄŌ²µ×ÉÕĘæÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ________£¬ĪŖ±£³Ö×°ÖĆCĪŖĪŽĖ®»·¾³£¬×°ÖĆBÖŠ¼ÓČėµÄŹŌ¼ĮŹĒ________”£
£Ø2£©ŹµŃé²½Öč£ŗČēĶ¼Į¬½Ó×°ÖĆŗó£¬ĻČ________£ØĢīŹµŃé²Ł×÷£©£¬ŌŁ×°Ņ©Ę·£¬Č»ŗóµćČ¼________£ØĢī”°A”±»ņ”°C”±£©“¦¾Ę¾«µĘ£¬µ±________£ØĢīŹµŃéĻÖĻó£©Ź±£¬ŌŁµćČ¼________£ØĢī”°A”±»ņ”°C”±£©“¦¾Ę¾«µĘ”£
£Ø3£©×°ÖĆDµÄ×÷ÓĆŹĒ________£¬________”£
£Ø4£©¼×Ķ¬Ń§ČĻĪŖ½ųČė×°ÖĆCµÄĘųĢåÖŠ»ģÓŠHCl£¬Ó¦ŌŚ×°ÖĆBĒ°Ōö¼Ó×°ÓŠ________£ØĢīŹŌ¼ĮĆū³Ę£©µÄĻ“Ęų×°ÖĆ³żČ„£»ŅŅĶ¬Ń§ČĻĪŖ²»ŠčŅŖ³żČ„HCl£¬ĄķÓÉĪŖ________”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com