
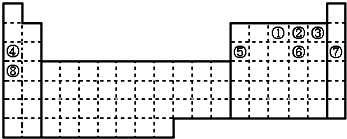
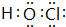
���� ��Ԫ�������ڱ���λ�ÿ�֪����ΪN����ΪO����ΪF����ΪNa����ΪAl����ΪS����ΪAr����ΪK��
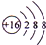
��1��������ΪS2-��������18�����ӣ���3�����Ӳ㣬���������Ϊ2��8��8��
��2�����Ӳ�ṹ��ͬ�����ӣ��˵����Խ�����Ӱ뾶ԽС�����ӵ��Ӳ�Խ�࣬���Ӱ뾶Խ��
��3���ǽ�����Խǿ����Ӧ�⻯��Խ�ȶ���
��4�����ͬһ���岢���ڶ����ڵ�Ԫ�ص�ij�ֺ������������ɱ����������ΪHClO��������Oԭ�ӷֱ���Hԭ�ӡ�Clԭ��֮���γ�1�Թ��õ��Ӷԣ�
��5������������������������������������ˮ����ΪKOH��Al������������Һ��Ӧ����ƫ�������������
��6������������ȼ�����ɹ������ƣ�ע�����ʵľۼ�״̬�뷴Ӧ����д�Ȼ�ѧ����ʽ��
��� �⣺��Ԫ�������ڱ���λ�ÿ�֪����ΪN����ΪO����ΪF����ΪNa����ΪAl����ΪS����ΪAr����ΪK��
��1��������ΪS2-��������18�����ӣ���3�����Ӳ㣬���������Ϊ2��8��8�����ӽṹʾ��ͼΪ�� ��
��
�ʴ�Ϊ�� ��
��
��2�����Ӳ�ṹ��ͬ�����ӣ��˵����Խ�����Ӱ뾶ԽС�����ӵ��Ӳ�Խ�࣬���Ӱ뾶Խ�����Ӱ뾶��r��N3-����r��O2-����r��Na+����r��Al3+����
�ʴ�Ϊ��r��N3-����r��O2-����r��Na+����r��Al3+����
��3���ǽ�����F��O���ǽ�����Խǿ����Ӧ�⻯��Խ�ȶ������⻯���ȶ��ԣ�HF��H2O��
�ʴ�Ϊ��HF��H2O��
��4�����ͬһ���岢���ڶ����ڵ�Ԫ�ص�ij�ֺ������������ɱ����������ΪHClO��������Oԭ�ӷֱ���Hԭ�ӡ�Clԭ��֮���γ�1�Թ��õ��Ӷԣ������ʽΪ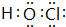 ��
��
�ʴ�Ϊ��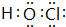 ��
��
��5��AlԪ���γɵ�����������������������������������ˮ����ΪKOH��Al������������Һ��Ӧ����ƫ���������������Ӧ���ӷ���ʽΪ��2Al+2OH-+2H2O=2AlO2-+3H2����
�ʴ�Ϊ��Al��2Al+2OH-+2H2O=2AlO2-+3H2����
��6������������ȼ�����ɹ������ƣ�2molNaȼ�շų�����Ϊ255.5kJ��2=511kJ����Ӧ�Ȼ�ѧ����ʽΪ��2Na��s��+O2��g��=Na2O2��s����H=-511kJ•mol-1��
�ʴ�Ϊ��2Na��s��+O2��g��=Na2O2��s����H=-511kJ•mol-1��
���� ���⿼��Ԫ�����ڱ���Ԫ��������Ӧ�ã���������Ԫ�����ڱ��Ľṹ�����������ʽΪ�״��㣬ѧ�������ܻ�ѧʽӰ�죬ע��Ի���֪ʶ���������գ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | BF3 | B�� | BeCl2 | C�� | PC13 | D�� | SO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
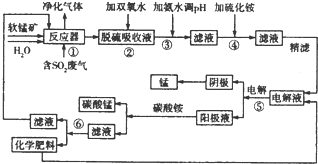
| ������ | Fe2+ | Fe3+ | Mn2+ | Ni2+ | Co2+ | |
| ����������� | ��ʼ������PH | 7.5 | 2.2 | 8.8 | 6.4 | 9.0 |
| ��ȫ������PH | 9.5 | 3.5 | 10.8 | 8.4 | ||
| ������� | ��ʼ������PH | 6.2 | 4.67 | |||
| ��ȫ������PH | ||||||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | P��Q��R��S��Ũ����� | B�� | P��Q��R��S�������й��� | ||
| C�� | P��Q�ķ�Ӧ��������ڲ� | D�� | P��Q��R��S��Ũ�Ȳ��ٱ仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ʯ��̼���ܻ�Ϊͬ�������� | B�� | N5��N2��Ϊͬ�������� | ||
| C�� | 14C��������Ϊ14 | D�� | �Ҵ��Ͷ���������ͬ���칹�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
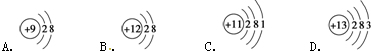
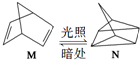 ��H=+88.6kJ•mol-1
��H=+88.6kJ•mol-1�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | X��Y�γɵ����ֻ����������������ӵĸ����Ⱦ�Ϊ2��1 | |
| B�� | Y���⻯���R���⻯���ȶ���Y���⻯���۷е��R���⻯��� | |
| C�� | Z��W��R����������Ӧˮ���������ǿ��˳��R��W��Z | |
| D�� | Y�ֱ���Z��W��R������Ԫ����ɵij�����������3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
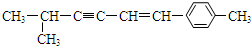 �����ڸ��л���Ŀռ乹������˵������ȷ���ǣ�������
�����ڸ��л���Ŀռ乹������˵������ȷ���ǣ�������| A�� | �÷��������е�̼ԭ�Ӿ����ܴ���ͬһƽ���� | |
| B�� | �÷�����һ�������̼ԭ��������Ϊ8�� | |
| C�� | �÷�����������9��̼ԭ�Ӵ���ͬһ��ֱ���� | |
| D�� | �÷����п��ܴ���ͬһƽ���ԭ���������Ϊ16�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com