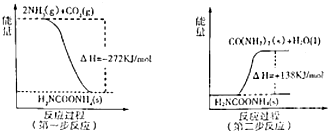
�������ڶ��ױ���������һ�������·���ȡ����Ӧ�����ȴ���A��A���������Ƶ�ˮ��Һ����ȡ����Ӧ���ɴ�B��B������������������ȩC��C������������������D��D�ʹ�����������Ӧ����DMP������DMP �Ľṹ֪�ڶ��ױ��м��������ӱ���ԭ��ȡ��������A�Ľṹ��ʽΪ��
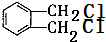
��B���ڶ����״���C���ڶ�����ȩ��D���ڶ������ᣬ�ڶ�������ʹ�����������Ӧ����DMP��DMP����Է�������Ϊ194����ô��Ǽ״���
����⣺�ڶ��ױ���������һ�������·���ȡ����Ӧ�����ȴ���A��A���������Ƶ�ˮ��Һ����ȡ����Ӧ���ɴ�B��B������������������ȩC��C������������������D��D�ʹ�����������Ӧ����DMP������DMP �Ľṹ֪�ڶ��ױ��м��������ӱ���ԭ��ȡ��������A�Ľṹ��ʽΪ��
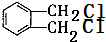
��B���ڶ����״���C���ڶ�����ȩ��D���ڶ������ᣬ�ڶ�������ʹ�����������Ӧ����DMP��DMP����Է�������Ϊ194����ô��Ǽ״���
��1��C���ڶ�����ȩ�����Ժ��еĹ�������ȩ�����ʴ�Ϊ��ȩ����
��2��A��DMP�ķ���ʽΪC
10H
10O
4���ʴ���
B��DMP�������������ͱ��������Կ��Է���ȡ�����ӳɡ������ȷ�Ӧ������ȷ��
C��DMP�������࣬������������ԭ��ֵ��DMP��ˮ�е��ܽ�Ȳ�����ȷ��
��ѡBC��
��3���ڶ����״����Ҷ��ᣨ

����һ�������¿������ʵ���1��1����������Ӧ���ɸ߷��ӻ������ṹ��ʽΪ��

��
�ʴ�Ϊ��

��
��4��

�ͼ״���һ�������·�����Ӧ����DMP��ˮ����Ӧ����ʽΪ��

��
�ʴ�Ϊ��

��
��5��C���ڶ�����ȩ�����㻯����E��C��Ϊͬ���칹�壬��lmolE������������Һ��Ӧȡ��2mol Ag����˵��E�к���1��ȩ������E���ܵĽṹ��ʽΪ

��
B���ڶ����״���BҲ���ڶ���ͬ���칹�壬B��ͬ���칹�����������������lmol�л��������2molNaOH��Ӧ��˵�������������ǻ����ڱ����ϵ�һ�ȴ���ֻ��һ�֣�
�����ϵ�����̼�ֱ���1.2.3.4.5.6��
��һ���칹��1.2����-OH��3.6��������
�ڶ����칹��1.2����-OH��4.5��������
�������칹��1.3����-OH��2.5��������
�������칹��1.4����-OH��2.6��������
�������칹��1.4����-OH��2.3��������
�������칹��1.4����-OH��2.5�����������Է���������һ����6�ֽṹ���ʴ�Ϊ��

��6��

 ������RΪ������ʵ���������·����ɵõ�DMP��
������RΪ������ʵ���������·����ɵõ�DMP��
 ����һ�������¿������ʵ���1��1������Ӧ���ɸ߷��ӻ�����ø߷��ӻ�����Ľṹ��ʽΪ
����һ�������¿������ʵ���1��1������Ӧ���ɸ߷��ӻ�����ø߷��ӻ�����Ľṹ��ʽΪ

 ��Ϊԭ��������������
��Ϊԭ�������������� ������ʹ����ij����һ�������·�Ӧ��ȡDMP��������ô���ȡDMP�Ļ�ѧ����ʽΪ
������ʹ����ij����һ�������·�Ӧ��ȡDMP��������ô���ȡDMP�Ļ�ѧ����ʽΪ



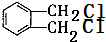 ��B���ڶ����״���C���ڶ�����ȩ��D���ڶ������ᣬ�ڶ�������ʹ�����������Ӧ����DMP��DMP����Է�������Ϊ194����ô��Ǽ״���
��B���ڶ����״���C���ڶ�����ȩ��D���ڶ������ᣬ�ڶ�������ʹ�����������Ӧ����DMP��DMP����Է�������Ϊ194����ô��Ǽ״���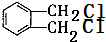 ��B���ڶ����״���C���ڶ�����ȩ��D���ڶ������ᣬ�ڶ�������ʹ�����������Ӧ����DMP��DMP����Է�������Ϊ194����ô��Ǽ״���
��B���ڶ����״���C���ڶ�����ȩ��D���ڶ������ᣬ�ڶ�������ʹ�����������Ӧ����DMP��DMP����Է�������Ϊ194����ô��Ǽ״��� ����һ�������¿������ʵ���1��1����������Ӧ���ɸ߷��ӻ������ṹ��ʽΪ��
����һ�������¿������ʵ���1��1����������Ӧ���ɸ߷��ӻ������ṹ��ʽΪ�� ��
�� ��
�� �ͼ״���һ�������·�����Ӧ����DMP��ˮ����Ӧ����ʽΪ��
�ͼ״���һ�������·�����Ӧ����DMP��ˮ����Ӧ����ʽΪ�� ��
�� ��
�� ��
�� ��6��
��6��

 ��У����ϵ�д�
��У����ϵ�д�