
| A. | 简单离子半径:W>Z>X | |
| B. | X、Y、Z都能与W组成离子化合物 | |
| C. | X、Y组成的化合物可与W单质反应 | |
| D. | Q是Z、W组成的化合物,1molQ中约含有6.02×1023个阴离子 |
分析 元素X、Y、Z位于不同短周期,原子序数依次增大,X、Y、Z分别位于第一、二、三周期,X只能H元素;X、Z同主族,则Z为Na元素;H、Na的原子序数之和是Y原子序数的两倍,则Y的原子序数=$\frac{1+11}{2}$=6,Y为C元素;主族元素W的原子最外层电子数比电子层数多4,当W含有2个电子层时,最外层含有6个电子,为C元素(Y为C元素,舍弃),当W位于第三周期时,最外层含有7个电子,为Cl元素,W不可能含有四个电子层,故W为Cl元素,据此进行解答.
解答 解:元素X、Y、Z位于不同短周期,原子序数依次增大,X、Y、Z分别位于第一、二、三周期,X只能H元素;X、Z同主族,则Z为Na元素;H、Na的原子序数之和是Y原子序数的两倍,则Y的原子序数=$\frac{1+11}{2}$=6,Y为C元素;主族元素W的原子最外层电子数比电子层数多4,当W含有2个电子层时,最外层含有6个电子,为C元素(Y为C元素,舍弃),当W位于第三周期时,最外层含有7个电子,为Cl元素,W不可能含有四个电子层,故W为Cl元素,
A.离子的电子层越多,离子半径越大,电子层相同时,核电荷数越大,离子半径越小,则离子半径大小为:W>Z>X,故A正确;
B.X、Y、Z分别为H、C、Na元素,W为Cl元素,H与Cl形成的HCl为共价化合物,故B错误;
C.X、Y分别为H、C元素,W的单质为氯气,C、H形成的烷烃、烯烃、炔烃等,烷烃能够与氯气发生取代反应,烯烃、炔烃与氯气能够发生加成反应,故C正确;
D.Q是Z、W组成的化合物,则Q为NaCl,1mol NaCl中含有1mol氯离子,约含有6.02×1023个阴离子氯离子,故D正确;
故选B.
点评 本题考查了原子结构与元素周期律的关系,题目难度中等,推断元素为解答关键,注意掌握原子结构与元素周期律、元素周期表的关系,试题培养了学生的分析能力及逻辑推理能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
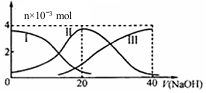 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中I代表H2A,II代表HAˉ,III代表A2ˉ).根据图判断,下列说法正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中I代表H2A,II代表HAˉ,III代表A2ˉ).根据图判断,下列说法正确的是( )| A. | 当V(NaOH)=20mL时,溶液中离子浓度大小关系:c(Na+)>c(A2-)>c(H+)>c(HA-)>c(OH-) | |
| B. | 等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水的大 | |
| C. | 当V(NaOH)=30 mL时,溶液中存在以下关系:2c(H+)+3c(H2A)+c(HA-)=c(A2-)+2c(OH-) | |
| D. | 向NaHA溶液加入水的过程中,pH可能增大也可能减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
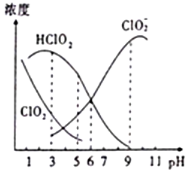 织物漂白剂亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都只有漂白作用,但ClO2是有毒气体.25℃时,各组分浓度随pH变化情况如图所示(Cl-没有画出).下列说法不正确的是( )
织物漂白剂亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都只有漂白作用,但ClO2是有毒气体.25℃时,各组分浓度随pH变化情况如图所示(Cl-没有画出).下列说法不正确的是( )| A. | 25℃时,ClO2-的水解平衡常数Ka=10-6 | |
| B. | 在pH约为4.0~4.5范围内使用该漂白剂较好 | |
| C. | 25℃时,等浓度的HClO2溶液和NaClO2溶液等体积混合后,混合溶液中:c(HClO2)+c(H+)+c(Na+)═c(ClO2-)+2c(OH-) | |
| D. | 当pH=5时往NaClO2溶液中滴入稀氢氧化钠溶液,溶液中主要反应的离子方程式是:HClO2+OH-═H2O+ClO2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 应用 | 解释 |
| A | 在相同条件下,在两支试管中各加入2mL 5% H2O2溶液,再向H2O2溶液中分别滴入1mL H2O和1mL 0.1mol•L-1 FeCl3溶液,对比观察现象 | 可以探究催化剂FeCl3对H2O2 分解速率的影响 |
| B | 向盛有1mL 0.01mol•L-1 AgNO3溶液的试管中滴加5滴0.01mol•L-1 NaCl溶液,有白色沉淀生成,再向其中滴加0.01mol•L-1 KI溶液,产生黄色沉淀. | 常温下,Ksp(AgCl)>Ksp(AgI) |
| C | 向两份蛋白质溶液中分别滴加饱和NaCl溶液和CuSO4溶液,均有固体析出 | 蛋白质均发生变性 |
| D | 保存硫酸亚铁溶液需加入少量稀盐酸和铁钉 | 防止 Fe2+水解以及被 O2 氧化 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
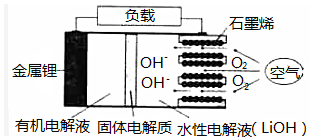 新型锂一空气电池具有能量密度高的优点,有望成为新能源汽车的电源,其结构如图所示,其中固体电解质只允许Li+通过.下列说法正确的是( )
新型锂一空气电池具有能量密度高的优点,有望成为新能源汽车的电源,其结构如图所示,其中固体电解质只允许Li+通过.下列说法正确的是( )| A. | 放电时,负极反应式:Li-e-+OH-═LiOH | |
| B. | 放电时,当外电路中有1mole-转移时,水性电解液离子总数增加NA | |
| C. | 应用该电池电镀铜,阴极质量增加64g,理沦上将消耗11.2LO2 | |
| D. | 若把水性电解液换成固体氧化物电解质,则易引起正极材料碳孔堵塞 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | NaOH | B. | NH3•H2O | C. | CuO | D. | Cu(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大气中大量的NO、NO2等酸性氧化物均是形成酸雨(PH>5.6)的主要原因 | |
| B. | 合成纤维,光导纤维,硝酸纤维均为有机高分子物质,用途广泛 | |
| C. | 二氧化硫和氯水均具有漂白性,可将两者混合使用增强漂白效果 | |
| D. | 地沟油,潲水油在餐饮企业中不能随意使用,但却可以用于制肥皂,变废为宝 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol•L-1的HF溶液加水稀释过程中,HF的电离平衡常数逐渐增大 | |
| B. | pH=12的NaOH溶液与pH=2的醋酸溶液等体积混合后,溶液呈中性 | |
| C. | pH=5的NaHSO3溶液中水电离出的H+浓度小于10-71mol•L-1 | |
| D. | 向Na2CO3,Na2SO4的混合溶液中逐滴加入BaCl2溶液,一定先生成BaSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S2-的结构示意图: | |
| B. | 乙烯的比例模型: | |
| C. | 乙醛的结构简式:CH3COH | |
| D. | 含中子数为10的氧元素的一种核素${\;}_8^{18}O$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com