
 ;由F生成一硝基产物的化学方程式为
;由F生成一硝基产物的化学方程式为 .
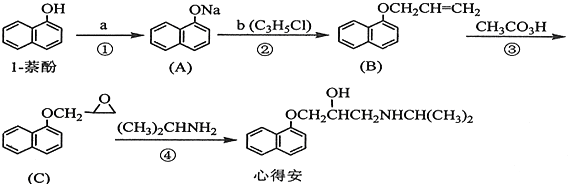
. 分析 由合成反应可知,反应①中酚-OH转化为-ONa,则试剂a为NaOH(或Na2CO3),由A、B的结构可知,反应②为取代反应,b为ClCH2CH=CH2,反应③中加氧去H为C=C的氧化反应,反应④为开环加成反应,结合心得安的结构简式确定分子式,以此解答(1)~(3);
(4)D是1-萘酚的同分异构体,其分子中有两个官能团,能发生银镜反应,则含-CHO;D能被KMnO4酸性溶液氧化成E(C2H4O2)和芳香化合物F(C8H6O4),E和F与碳酸氢钠溶液反应均能放出CO2气体,E、F均含-COOH,则D中含-C≡C-CH3,F芳环上的一硝化产物只有一种,F为对二苯甲酸,则D中-CHO、-C≡C-CH3在苯环的对位,以此来解答.
解答 解:由合成反应可知,反应①中酚-OH转化为-ONa,则试剂a为NaOH(或Na2CO3),由A、B的结构可知,反应②为取代反应,b为ClCH2CH=CH2,反应③中加氧去H为C=C的氧化反应,反应④为开环加成反应,
(1)由上述分析可知,a为NaOH(或Na2CO3),b为ClCH2CH=CH2,b中官能团为氯原子、碳碳双键,
故答案为:NaOH(或Na2CO3);氯原子、碳碳双键;
(2)由上述分析可知反应②为取代反应,故答案为:取代反应;
(3)由心得安的结构简式可知分子式为C16H21O2N,
故答案为:C16H21O2N;
(4)D是1-萘酚的同分异构体,其分子中有两个官能团,能发生银镜反应,则含-CHO;D能被KMnO4酸性溶液氧化成E(C2H4O2)和芳香化合物F(C8H6O4),E和F与碳酸氢钠溶液反应均能放出CO2气体,E、F均含-COOH,则D中含-C≡C-CH3,F芳环上的一硝化产物只有一种,F为对二苯甲酸( ),则D中-CHO、-C≡C-CH3在苯环的对位,所以D的结构简式为
),则D中-CHO、-C≡C-CH3在苯环的对位,所以D的结构简式为 ,由F生成的一硝化产物的化学方程式为
,由F生成的一硝化产物的化学方程式为 ,
,
故答案为: ;
; .
.
点评 本题侧重有机合成的考查,把握合成流程中结构、官能团的变化为解答的关键,明确官能团与性质的关系、反应条件和反应类型的关系、同分异构体的推断即可解答,题目难度中等.


 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:解答题
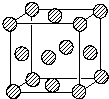 前四周期原子序数依次增大的六种元素,A、B、C、D、E、H中,A元素在宇宙中含量最丰富,B元素基态原子的核外有3种能量不同的原子轨道,且每种轨道中的电子数目相同.D元素是地壳中含量最多的元素,E为d区元素,其外围电子排布中有4对成对电子,H元素基态原子最外层只有一个电子,其它层均已充满电子.
前四周期原子序数依次增大的六种元素,A、B、C、D、E、H中,A元素在宇宙中含量最丰富,B元素基态原子的核外有3种能量不同的原子轨道,且每种轨道中的电子数目相同.D元素是地壳中含量最多的元素,E为d区元素,其外围电子排布中有4对成对电子,H元素基态原子最外层只有一个电子,其它层均已充满电子.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
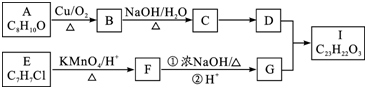
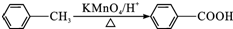
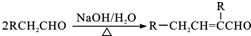
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+中质子数与电子数 | B. | NH4HSO4晶体中阳离子与阴离子 | ||
| C. | OH-中电子数与中子数 | D. | Na2O2中阳离子与阴离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4和C3H6 | B. | CH4和C2H4 | C. | CH4和C3H8 | D. | CH4和C4H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
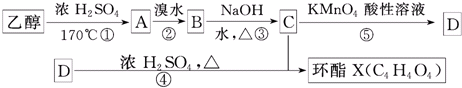
 +2H2O
+2H2O查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 苯和油脂均不能使酸性KMnO4褪色 | |
| B. | CH2Cl2只有一种结构说明甲烷分子是正四面体结构,而不是平面正方形结构 | |
| C. | 蒸馏和分馏都是通过沸点不同分离液态混合物的 | |
| D. | 油脂皂化反应的产物是高级脂肪酸和甘油 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
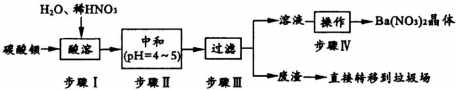
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com