
| A、炭在常温下化学性质不活泼,因此在埋木桩前,可将埋入地下的一段表面用火微微烧焦 |
| B、碳酸钠的水溶液呈碱性,医学上能用于治疗胃酸过多 |
| C、盐酸与苛性钠可自发进行反应,该反应可以设计成原电池 |
| D、次氯酸具有强氧化性,可以起到除去水中悬浮的杂质和杀菌消毒作用 |


科目:高中化学 来源: 题型:
| A、1:10:1010:109 |
| B、1:5:5×109:5×106 |
| C、1:20:1010:107 |
| D、1:10:102:107 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠、镁、铁对应的氧化物都是碱性氧化物 |
| B、食醋、纯碱、食盐分别属于酸、碱、盐 |
| C、生铁、不锈钢、青铜都属于合金 |
| D、明矾、小苏打、水玻璃、次氯酸均为电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
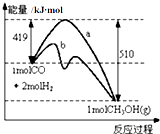 工业上用CO生产燃料甲醇.一定温度和容积条件下发生反应:CO(g)+2H2(g)CH3OH(g).如图表示反应中的能量变化; 请回答下列问题:
工业上用CO生产燃料甲醇.一定温度和容积条件下发生反应:CO(g)+2H2(g)CH3OH(g).如图表示反应中的能量变化; 请回答下列问题:| 3 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D |
| E | F |
| 物质 | X | Y | Z | W |
| 起始投料/mol | 2 | 1 | 2 | 0 |
| 实验序号 | ① | ② | ③ |
| 压强p/Pa | 1×105 | 2×105 | 1×106 |
| c(Y)/mol?L-1 | 0.08 | 0.12 | 0.68 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将pH=4的盐酸和醋酸稀释成pH=5的溶液,盐酸加水后体积为原溶液的10倍,醋酸所需加入的水量比前者多 |
| B、盐酸和醋酸都可用相应的钠盐与浓硫酸反应制取 |
| C、相同pH的盐酸和醋酸溶液中分别加入相应的钠盐固体,醋酸的pH变大 |
| D、pH值相同的盐酸和醋酸分别跟锌反应时,产生氢气的起始速率相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com