
| A. | 浓H2SO4 | B. | HNO3 | C. | HCl | D. | H2O |
科目:高中化学 来源: 题型:选择题
| A. | 振荡试管中的液体时,应用手指拿住试管,用手腕甩动 | |
| B. | 在做乙烯的制备实验时要加少量的碎瓷片,以防止溶液暴沸 | |
| C. | 因苯酚具有弱酸性,如果皮肤上不慎沾有苯酚,应立即用大量的NaOH稀溶液冲洗 | |
| D. | 中学阶段在使用试剂时,应先用蒸馏水湿润,然后再将待测液滴到试纸上,看变化的结果,但是pH试纸除外,在使用时不能先用蒸馏水润湿 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=5的H2S溶液中,c(H+)=c(HS-)=1×10-5mol•L-1 | |
| B. | pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1 | |
| C. | pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+c(H+)=c(OH-)+c( HC2O4-) | |
| D. | 相同浓度的三种溶液①CH3COONa ②NaHCO3③NaClO的pH大小比较:③>②>① |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用物质A表示的反应的平均速率为0.2mol•L-1•s-1 | |
| B. | 用物质B表示的反应的平均速率为0.1mol•L-1•s-1 | |
| C. | 2s时物质A的转化率为70% | |
| D. | 2s时物质B的浓度为0.7mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有Fe3+的溶液:Na+、SCN-、Cl-、S2- | |
| B. | 含有大量NO3-的溶液:H+、SO32-、Cl-、SO42- | |
| C. | 常温下,pH=12的溶液:K+、Cl-、CO32-、AlO2- | |
| D. | 与铝反应产生无色无味气体的溶液:NO3-、K+、Cl-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X、Y、Z的稳定性逐渐增强 | B. | A、B、C、D只能形成5种单质 | ||
| C. | X、Y、Z在常温下均为气态 | D. | A、B、C、D的电负性逐渐增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 严格执行机动车尾气排放标准有利于防止大气污染 | |
| B. | 使用二氧化硫增白的食品对人体健康产生损害 | |
| C. | 使用氯气对自来水消毒时生成的有机氯化物可能对人体有害 | |
| D. | 食品厂产生的含丰富氮、磷营养素的废水可长期排向水库养鱼 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解质的溶解开始后,只有电解质的溶解过程,没有电解质的析出过程 | |
| B. | 沉淀溶解达到平衡时,沉淀的速率和溶解的速率相等 | |
| C. | 沉淀溶解达到平衡时,溶液中溶质的离子浓度相等,且保持不变 | |
| D. | 沉淀溶解达到平衡时,如果再加入难溶性的该沉淀物,将促进溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
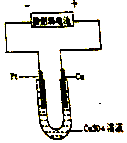 肼(N2H6)又称联氨,是一种可燃性的液体,可用作火箭燃料.
肼(N2H6)又称联氨,是一种可燃性的液体,可用作火箭燃料.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com