
| A | B | C | |
| ① | NaOH溶液 | Al(OH)3 | 稀硫酸 |
| ② | KOH溶液 | SiO2 | 稀盐酸 |
| ③ | O2 | N2 | H2 |
| ④ | FeCl3溶液 | Cu | 浓硝酸 |
| A. | ①③ | B. | ①④ | C. | ②④ | D. | ②③ |
分析 ①氢氧化铝具有两性,既能与氢氧化钠反应又能与硫酸反应;
②SiO2属于酸性氧化物,能和强碱溶液反应,但不能和稀盐酸反应;
③氮气和氢气、氧气都能反应,但常温下不反应;
④Cu能被强氧化剂硝酸氧化、也能被氯化铁氧化.
解答 解:①氢氧化铝具有两性,既能与氢氧化钠反应又能与硫酸反应,Al(OH)3+NaOH=NaAlO2+2H2O、2Al(OH)3+3H2SO4=Al2(SO4)3+6H2O,故正确;
②SiO2属于酸性氧化物,能和强碱溶液反应,但不能和稀盐酸反应,SiO2+2NaOH=Na2SiO3+H2O,故错误;
③氮气和氢气、氧气都能反应,但常温下不反应,N2+O2$\frac{\underline{\;放电\;}}{\;}$2NO、N2+3H2$\frac{\underline{\;\;\;催化剂\;\;\;}}{高温高压}$2NH3,故错误;
④Cu能被强氧化剂硝酸氧化、也能被氯化铁氧化,Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O、2FeCl3+Cu=CuCl2+2FeCl2,故正确;
故选B.
点评 本题考查物质之间的反应,明确物质的性质是解本题关键,注意结合题给信息解答,有些物质之间能反应,但常温下不反应,为易错点.


科目:高中化学 来源: 题型:选择题
| 实验事实 | 结论 | |
| A | Cl2的水溶液可以导电 | Cl2是电解质 |
| B | SO2通入硝酸钡溶液出现白色沉淀 | BaSO3不溶于强酸 |
| C | NaHCO3溶液与NaAlO2溶液混合产生白色沉淀 | 酸性:HCO3->Al(OH)3 |
| D | 常温下白磷可自燃而N2须在放电时才与O2反应 | 非金属性:P>N |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2g H2含有的氢原子数目为NA | |
| B. | 常温常压下,22.4 LO2含有的分子数目为NA | |
| C. | 1 molZn转变为Zn2+失去的电子数目为NA | |
| D. | 1 L 1mol•L-1KOH溶液中含有的钾离子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气与石灰乳反应制漂白粉 | B. | 钠在氯气中燃烧生成氯化钠 | ||
| C. | 氯化铵与氢氧化钙共热制氨气 | D. | 浓盐酸与二氧化锰共热制氯气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,预测该芳香烃能(填“能”或“不能”)发生该类反应.
,预测该芳香烃能(填“能”或“不能”)发生该类反应.
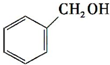 c.
c.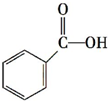
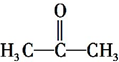
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜属于重金属,但其盐有毒,所以铜质器皿不安全,应该禁用 | |
| B. | 食盐、食醋和味精是常用的食品添加剂,其主要化学成分均属钠盐 | |
| C. | 氨气液化以及液氨气化均要吸收大量的热,所以氨常用于制冷剂 | |
| D. | SO2能使食物增白,但这类食物会严重损害人体的肝肾,所以食品中应该严格限量使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 物质 | 杂质 | 除杂试剂 | 反应条件或除杂方法 |
| A | 苯 | 乙酸 | 烧碱溶液 | 分液 |
| B | 硅 | 铝 | 稀盐酸 | 过滤 |
| C | 氯气 | 氯化氢 | 饱和食盐水 | 洗气 |
| D | 乙烷 | 乙烯 | 氢气 | 催化剂、加热 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
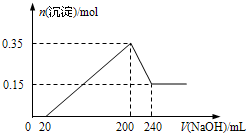 将一定质量的Mg和Al的混合物投入500mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.则下列说法正确的是( )
将一定质量的Mg和Al的混合物投入500mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.则下列说法正确的是( )| A. | Mg和Al的总质量为8 g | |
| B. | 硫酸的物质的量浓度为5 mol/L | |
| C. | NaOH溶液的物质的量浓度为5 mol/L | |
| D. | 生成的H2在标准状况下的体积为11.2 L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com