
(1)在与外界隔离的体系中,自发过程将导致体系的熵 ,(填“增大”、“减小”、“不变”);对于同一种物质, 时熵值最大。(填“固态”、“液态”、“气态”)
(2)某工厂实验室用CO和H2制备CH3OH,其原理为:CO(g)+2H2(g)  CH3OH(g) △H < 0该温度下的化学平衡常数表达式_____________;若在298K、398K时化学平衡常数分别为K1、K2,则K1 K2(填“>”、“<”、“=”)
CH3OH(g) △H < 0该温度下的化学平衡常数表达式_____________;若在298K、398K时化学平衡常数分别为K1、K2,则K1 K2(填“>”、“<”、“=”)
(3)M与N是同素异形体,由M=N;△H=+119KJ/mol可知,M比N________(填稳定、不稳定)
(4)一定温度下,反应3Fe(s)+4H2O(g)?Fe3O4(s)+4H2(g),在一密闭容器中进行达平衡后, 保持压强不变,充入Ar,其正反应速率__________(A.变快 B.不变 C变慢,填字母代号);该反应向__________(填正移、逆移或不移)。
科目:高中化学 来源:2016-2017学年黑龙江哈尔滨六中高一上期中化学试卷(解析版) 题型:选择题
下列说法中正确的是( )
A.同温同压下,相同体积的物质,它们的物质的量必相等
B.1 L一氧化碳气体一定比1 L氧气的质量小
C.28 g N2和CO的混合气体在标准状况下的体积约为22.4 L
D.常温常压下,1 mol碳完全燃烧消耗22.4 L氧气
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江哈尔滨六中高二上期中化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.需要加热的反应一定是吸热反应
B.所有的化学反应都有能量变化
C.所有的放热反应都可以在常温常压下自发进行
D.核能作为一种反应热,是理想的新能源
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆中学高一上期中化学试卷(解析版) 题型:选择题
关于溶液、胶体和浊液下列说法正确的是:
A.溶液稳定,胶体和浊液都不稳定
B.溶液中的分散质能通过滤纸但不能通过半透膜
C.溶液和胶体的本质区别在于是否能产生丁达尔效应
D.NaCl溶液和CaCO3悬浊液的本质区别是分散质粒子的大小
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆中学高一上期中化学试卷(解析版) 题型:选择题
①试管 ②烧杯 ③酒精灯 ④试管夹 ⑤石棉网 ⑥泥三角 ⑦坩埚 ⑧铁三脚架
A. ③⑥⑦⑧ B. ②③⑤⑧ C. ①③④⑤ D. ②③⑤⑥
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆中学高二上期中化学试卷(解析版) 题型:选择题
在一定温度下,在某密闭容器内某一反应中M、N的物质的量随反应时间变化的曲线如图所示.下列叙述中,正确的是( )
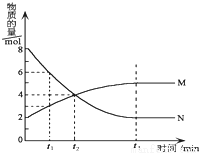
A.该反应的化学方程式为M═2N
B.若t1=1,则反应开始至t1时间段M 的反应速率为1mol﹒L-1﹒min-1
C.t3时正反应速率等于逆反应速率
D.t2时正逆反应速率相等,反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆中学高二上期中化学试卷(解析版) 题型:选择题
硫代硫酸钠(Na2S2O3)与稀H2SO4溶液反应:Na2S2O3+H2SO4=Na2SO4+SO2↑十S↓+H2O下列化学反应速率最大的是 ( )
A.0.1mol/L Na2S2O3和0.1mol/L H2SO4溶液各5ml,加水5ml,反应温度10℃
B.0.1mol/L Na2S2O3和0.1mol/L H2SO4溶液各5ml,加水10ml,反应温度10℃
C.0.1mol/L Na2S2O3和0.1mol/L H2SO4溶液各5ml,加水10ml,反 应温度30℃
应温度30℃
D.0.2mol/L Na2S2O3和0.1mol/L H2SO4溶液各5ml,加水10ml,反应温度30℃
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆一中高二上10月月考化学卷(解析版) 题型:选择题
将2mol A和2molB充入到绝热恒容密闭容器中,发生如下反应:2A(g)+B(g) 3C(g)+D(s),达到平衡测得容器内压强增大,若该反应在恒温恒容的密闭容器中进行,下列有关说法正确的是
3C(g)+D(s),达到平衡测得容器内压强增大,若该反应在恒温恒容的密闭容器中进行,下列有关说法正确的是
A.平衡前,随着反应的进行,容器内压强始终不变
B.平衡时,分离出少量D,A的转化率提高
C.平衡时,升高温度,容器内混合气体的密度减小
D.平衡时,充入C,该反应平衡常数减小
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高二上期中化学试卷(解析版) 题型:选择题
已知常温常压下,P2和P4燃烧的热化学方程式分别为:
2P2(g)+5O2(g)=P4O10(s)ΔH=-2695.4kJ·mol-1,
P4(g)+5O2(g)=P4O10(s)ΔH=-2925.1kJ·mol-1。则下列说法正确的是
A.2P2(g)=P4(g)ΔH=+229.7kJ·mol-1
B.P2制P4是放热反应
C.P2比P4更加稳定
D.等质量时,P2比P4具有的能量高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com