
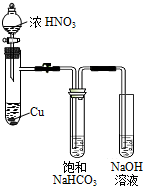
 某化学学习小组发现在碱性溶液中,NO2会发生如下反应:
某化学学习小组发现在碱性溶液中,NO2会发生如下反应:分析 (1)①碳酸氢钠溶液中碳酸氢根离子水解溶液显碱性;
(2)②二氧化氮与水反应生成硝酸;
③NO2与NaHCO3溶液反应生成NaNO2,此时氮的化合价降低,根据氧化还原反应的原理可知,还应有硝酸根生成;
④X中既有NaNO2又有NaNO3,在酸性条件下都能氧化碘离子;
⑤称取a gKMnO4固体,加蒸馏水和少量稀硫酸溶解,配成250mL溶液.移取20.00mL X于锥形瓶,用所配的酸性KMnO4溶液进行滴定,消耗b mL KMnO4溶液,根据反应5NO2-+2MnO4-+6H+═5NO3-+2Mn2++3H2O,利用高锰酸钾的物质的量可计算出X中所含有的NaNO2的物质的量,进而确定NaNO2的浓度.
解答 解:(1)①碳酸氢钠溶液中碳酸氢根离子水解沉淀大于电离程度,溶液显碱性,HCO3-+H2O?H2CO3+OH-,
故答案为:碳酸氢根离子水解沉淀大于电离程度,溶液显碱性,HCO3-+H2O?H2CO3+OH-;
(2)②二氧化氮与水反应也能生成硝酸根,所以检验X中存在NO3-不能说明是NO2和NaHCO3溶液反应生成了硝酸根,
故答案为:二氧化氮与水反应也能生成硝酸根;
③NO2与NaHCO3溶液反应生成NaNO2,此时氮的化合价降低,根据氧化还原反应的原理可知,还应有硝酸根生成,所以NO2与NaHCO3溶液反应的化学方程式为2NO2+2NaHCO3═NaNO2+NaNO3+2CO2↑+H2O,反应的离子方程式为:2NO2+2HCO3-═NO2-+NO3-+2CO2↑+H2O,
故答案为:2NO2+2HCO3-═NO2-+NO3-+2CO2↑+H2O;
④X中既有NaNO2又有NaNO3,NaNO2和NaNO3在酸性条件下都能氧化碘离子生成碘单质,所以不能用KI淀粉溶液检验X中存在NaNO2,
故答案为:不能;NaNO2和NaNO3在酸性条件下都能氧化碘离子生成碘单质;
⑤称取a gKMnO4固体,加蒸馏水和少量稀硫酸溶解,配成250mL溶液.移取20.00mL X于锥形瓶,用所配的酸性KMnO4溶液进行滴定,消耗b mL KMnO4溶液,高锰酸钾的物质的量为$\frac{ag}{158g/mol}$×$\frac{b}{250}$,根据反应5NO2-+2MnO4-+6H+═5NO3-+2Mn2++3H2O,可知20.00mL X溶液中所含有的NaNO2的物质的量为$\frac{ag}{158g/mol}$×$\frac{b}{250}$×$\frac{5}{2}$=$\frac{ab}{15800}$mol,
所以NaNO2的浓度为=$\frac{\frac{ab}{15800}mol}{0.020L}$=$\frac{ab}{316}$mol/L,
故答案为:$\frac{ab}{316}$mol/L.
点评 本题考查较为综合,以物质的制备实验为载体,综合考查实验的设计、物质的检验、氧化还原滴定等知识,注意根据物质的性质设计实验方案,题目难度中等.


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 +NaOH$\stackrel{H_{2}O}{→}$
+NaOH$\stackrel{H_{2}O}{→}$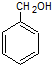 +NaCl,反应类型为取代反应.
+NaCl,反应类型为取代反应. .
. .
.

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 进行蒸发操作时,当溶液中出现较多固体时即可停止加热 | |
| B. | 进行蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 进行分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 进行萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 40和120 | B. | 65和90 | C. | 40和90 | D. | 90和120 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 乙醇中含有少量水可加入生石灰再蒸馏制得无水乙醇 | |
| B. | 将无水乙醇和浓硫酸按体积比3:1混合,加热至170℃制取乙烯 | |
| C. | 蔗糖水解用浓硫酸作催化剂 | |
| D. | 油脂皂化反应后,反应混合物中加入食盐可将肥皂分离出来 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石英玻璃具有固定的熔点 | |
| B. | 石英玻璃的结构类似于液体 | |
| C. | 石英玻璃耐高温且能抵抗一切酸的腐蚀 | |
| D. | 石英玻璃能经受温度剧变且能抵抗碱的腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 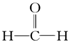 醛类 醛类 | B. | 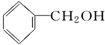 酚类-OH 酚类-OH | C. |  醛类 醛类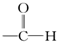 | D. | CH3COOCH3羧酸类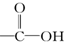 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com