
分析 利用置换反应Zn+CuSO4=ZnSO4+Cu,说明Zn和Cu的金属活动性顺序,据此设计原电池时,根据反应可知,Zn为负极,则正极可以是活泼性不如Zn的金属如Cu等,也可以是碳棒,电解质溶液应为CuSO4,工作时,正极反应式为Cu2++2e-=Cu,有红色金属析出,负极反应式为Zn-2e-=Zn2+,Zn棒逐渐溶解.
解答 解:(1)利用反应Zn+CuSO4=ZnSO4+Cu设计原电池时,根据反应可知,Zn为负极,则正极可以是活泼性不如Zn的金属如Cu等,也可以是碳棒,电解质溶液应为CuSO4,故答案为:铜片;锌片;
(2)原电池工作时,正极反应式为Cu2++2e-=Cu,负极反应式为Zn-2e-=Zn2+,故答案为:Cu2++2e-=Cu;Zn-2e-=Zn2+;
(3)正极发生还原反应,生成红色金属铜,溶液蓝色变浅.负极发生氧化反应,锌逐渐溶解,故答案为:负极不断溶解,正极上有红色固体析出,溶液蓝色变浅;
(4)锌逐渐溶解,正极析出红色金属铜,说明金属活动性Zn>Cu,故答案为:金属活动性Zn>Cu.
点评 本题考查原电池的设计和工作原理,题目难度不大,注意原电池正负极材料及电解质溶液的选择.


 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:解答题
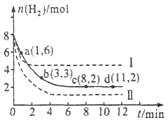 工业上有一种用CO2来生产甲醇燃料的方法:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1
工业上有一种用CO2来生产甲醇燃料的方法:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸馏法是海水淡化的方法之一 | |
| B. | 长期饮用纯净水,可能会引起一些微量元素的缺乏 | |
| C. | 含有细菌的水可以用臭氧杀菌 | |
| D. | 含有重金属离子的废水用可以用明矾处理 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(NH3)=0.1 mol/(L•min) | B. | v(NH3)=0.2 mol/(L•min) | ||
| C. | v(H2)=0.3 mol/(L•min) | D. | v(H2)=0.4 mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
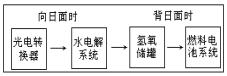 如图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH溶液为电解液,下列有关说法中不正确的是( )
如图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH溶液为电解液,下列有关说法中不正确的是( )| A. | 该能量转化系统中的水也是可能循环的 | |
| B. | 燃料电池系统产生的能量实际上来自于水 | |
| C. | 水电解系统中的阳极有O2放出 | |
| D. | 燃料电池放电时的负极反应:H2+2OH--2e-=2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体带电荷,溶液不带电荷 | |
| B. | 胶体区别于其它分散系的本质特征是分散质的直径大小 | |
| C. | 将一柬光线通过胶体时可出现一条光亮的通路,通过溶液则没有此现象 | |
| D. | 土壤胶粒的表面巨大且带负电,能吸附NH${\;}_{4}^{+}$等营养离子,使土壤具有保肥能力 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al2(SO4)3、NaOH | B. | Al2(NH3)2OH、KOH | C. | BaCl2、NaHCO3 | D. | Ca(ClO)2、NaHSO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用醋酸除去水垢中的碳酸钙:CaCO3+2H+=Ca2++H2O+CO2↑ | |
| B. | 石灰水中加入过量小苏打溶液:HCO3-+Ca2++OH-=CaCO3↓+H2O | |
| C. | 解饱和NaCl饱和溶液:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑ | |
| D. | 铝溶于氢氧化钠溶液:Al+2OH-+H2O=AlO2-+2H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质的量是用来研究微观粒子的一个国际基本物理量,其单位处摩尔 | |
| B. | 气体的摩尔体积与温度和压强有关,压强越大,体积越大 | |
| C. | 若x个N (氮)原子的质级是1克,则阿伏加德罗常数可表示为14x/mol | |
| D. | 任何一种微观粒子,当摩尔质量以g/mol为单位时,其数值与这种粒子的相对分子质量或相对原子质量相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com