


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②⑤ | B、③⑤⑥ |
| C、③⑤ | D、②⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、所用NaOH已吸潮 |
| B、摇匀后液面低于刻度线,不再补加水 |
| C、有少量NaOH溶液残留在烧杯内 |
| D、向容量瓶加水至时刻度线时俯视液面 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在常温下AgI水溶液中,Ag+和I-浓度的乘积是一个常数 |
| B、在常温下,在任何含AgI固体的溶液中,c(Ag+)=c(I-)且Ag+与I-浓度的乘积等于8.3×10-17 mol2?L-2 |
| C、常温下,将1mL 1.0×10-2 mol/L的KI与AgNO3溶液等体积混合,则生成AgI沉淀所需AgNO3溶液的最小浓度为3.32×10-14mol/L |
| D、向AgI饱和溶液中加入AgBr固体,c(I-)不变,Ksp值不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| PH t/min T/℃ | 3.0 | 4.0 | 5.0 | 6.0 |
| 20 | 301 | 231 | 169 | 58 |
| 30 | 158 | 108 | 18 | 15 |
| 50 | 31 | 26 | 15 | 7 |
| A | B | C | D |
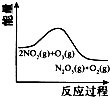 |  |  | 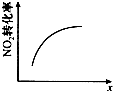 |
| 升高温度,平衡常数减小 | 0~3s内,反应速率为v(NO2)=0.2mol?L-1?s-1 | t1时仅加入催化剂,平衡正向移动 | 达平衡时,仅改变x,则x为c(O2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH相等的①NH4Cl ②(NH4)2SO4 ③NH4HSO4溶液,NH4+大小顺序为①>②>③ |
| B、pH相等的NaF与CH3COOK溶液:[c(Na+)-c(F-)]>[c(K+)-c(CH3COO-)] |
| C、0.2 mol?L-1的Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3) |
| D、0.2 mol?L-1 HCl与0.1 mol?L-1 NaAlO2溶液等体积混合:c(Cl-)>c(Na+)>c(Al3+)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、当氢氟酸溶液温度升高,HF的电离程度减小(不考虑挥发) |
| B、水电离的热化学方程式为:H2O(1)?H+(aq)+OH-(aq)△H=+57.3kJ/mol |
| C、当c>0.1时,一定不存在:c(Na+)=c(F-) |
| D、若混合后溶液中:c(Na+)>c(OH-)>c(F-)>c(H+),则c一定小于0.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ① |
| ② |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com