
化学与生活密切相关,下列说法正确的是( )
A.蛋白质和油脂都是天然高分子化合物
B.CO2和CH4都是造成温室效应的气体
C.蔗糖和麦芽糖的水解产物均为葡萄糖
D.苯酚和甲苯遇FeCl3均显紫色
科目:高中化学 来源: 题型:
两种元素原子的核外电子层数之比与最外层电子数之比相等,则在周期表的前10号元素中,满足上述关系的元素共有( )
A.1对 B.2对 C.3对 D.4对
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z均为短周期主族元素,其核电荷数依次增大,且它们的原子最外层电子数之比为1∶4∶2。下列叙述中正确的是( )
A.X一定是碱金属元素
B.Y元素能形成化合物NaHYO3,且其水溶液呈碱性
C.Z元素形成的最高价氧化物熔点较低
D.X的单质一定能通过电解Z的盐酸盐溶液制备
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.煤的液化和气化都是物理变化
B.乙醇、乙酸和甲醛广泛应用于食品加工
C.蛋白质、橡胶和塑料都是天然高分子
D.高铁车厢大部分材料采用铝合金,因铝合金强度大、质量轻、抗腐蚀能力强
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关有机物性质的说法正确的是( )
A.蛋白质可以与酸、碱或重金属盐反应
B.芳香烃都不能使酸性KMnO4溶液褪色
C.CH3CH2OH与氢溴酸能反应
D.石油的分馏可获得乙烯、丙烯等不饱和烃
查看答案和解析>>
科目:高中化学 来源: 题型:
汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3===K2O+5Na2O+16N2↑。若氧化产物比还原产物多1.75 mol,则下列判断正确的是( )
A.生成42.0 L N2(标准状况)
B.有0.250 mol KNO3被氧化
C.转移电子的物质的量为1.25 mol
D.氧化产物的物质的量为3.75 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有_______________________________________
________________________________________________________________________。
(2)硫酸铜溶液可以加快氢气生成速率的原因是______________________________
________________________________________________________________________。
(3)实验室中现有Na2SO4、MgSO4、Ag2SO4、K2SO4等4种溶液,可与上述实验中CuSO4溶液起相似作用的是________。
(4)要加快上述实验中气体产生的速率,还可采取的措施有______________________________(答两种)。
(5)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列的实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
| 实验 混合溶液 | A | B | C | D | E | F |
| 4 mol·L-1 H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
①请完成此实验设计,其中:V1=__________________,V6=__________,V9=________;
②反应一段时间后,实验A中的金属呈________色,实验E中的金属呈________色;
③该同学最后得出的结论为当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因:________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某原电池装置如图所示,电池总反应为2Ag+Cl2===2AgCl。下列说法正确的是( )
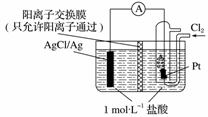
A.正极反应为AgCl+e-===Ag+Cl-
B.放电时,交换膜右侧溶液中有大量白色沉淀生成
C.若用NaCl溶液代替盐酸,则电池总反应随之改变
D.当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com