
| A. | 研究物质的性质时,常用到观察、实验、分类、比较、模型、假设等方法 | |
| B. | 研究物质性质的一般程序的第二步是观察物质的外观 | |
| C. | 可以用分类的方法预测物质的性质 | |
| D. | 观察是一种有计划、有目的地用感官考察研究对象的方法 |
分析 A.化学研究的基本方法有:观察、实验、分类、比较等方法,除此之外,建立假说和化学模型在研究物质的结构和性质时也起着重要的作用;
B.研究物质性质的基本程序为:观察物质的外观性质、预测物质的性质、实验和观察、解释和结论;
C.不同物质类别的物质,具有的通性不同,依据物质通性预测物质具有的性质;
D.观察法的含义:即仔细观看客观事物或现象.是一种有计划、有目的地用感官考察研究对象的方法.
解答 解:A.观察、实验、分类、比较、模型、假设等方法是研究物质性质的基本方法,故A正确;
B.探究物质性质的基本程序是观察物质的外观性质、预测物质的性质、实验和观察、解释和结论,研究物质性质的一般程序的第一步是观察物质的外观,故B错误;
C.相同类别的物质的性质相似,可用分类的方法预测,故C正确;
D.观察法的含义:即仔细观看客观事物或现象.是一种有计划、有目的地用感官考察研究对象的方法.故D正确.
故选B.
点评 本题考查了化学研究的基本方法和作用,有利于培养学生良好的科学素养,提高学习的积极性,题目难度不大,侧重对基础知识的巩固,注意对基础知识的理解掌握.


 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选 项 | 操 作 | 现 象 | 结 论 |
| A | 向无水乙醇中滴入酸性KMnO4溶液,充分振荡 | 紫红色褪去 | 乙醇有氧化性 |
| B | 向某溶液中滴加BaCl2溶液 | 生成白色沉淀 | 原溶液中一定有SO42- |
| C | 向某无色溶液中滴加氯水和CCl4,振荡、静置 | 下层溶液显紫色 | 原溶液中有I- |
| D | 向某溶液中滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
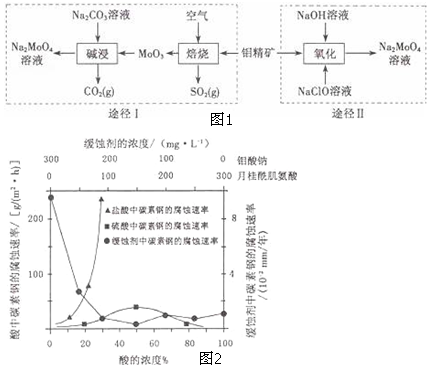
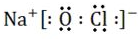 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
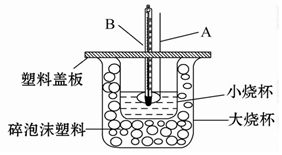
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 操作 | 现象 | 结论 | |
| A | 滴加稀盐酸 | 有气泡产生 | 原溶液中有CO32- |
| B | 滴加盐酸酸化的BaCl2溶液 | 生成白色沉淀 | 原溶液中有Ag+或SO42- |
| C | 用洁净铂丝蘸取溶液进行灼烧 | 火焰呈黄色 | 原溶液中有Na+、无K+ |
| D | 滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管 | 试纸不变蓝 | 原溶液中无NH4+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气可用于自来水消毒 | |
| B. | 40%的甲醛水溶液可用作防腐剂,浸制生物标本 | |
| C. | 工业酒精可用于酿造饮用酒 | |
| D. | 食盐中添加碘酸钾(KIO3)加工碘盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
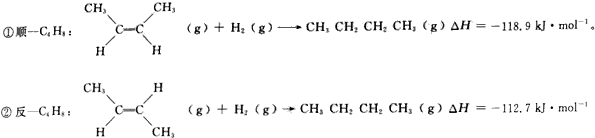


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com