
| A. | 1mol 12C原子的质量是12g,1个12C原子的质量是$\frac{12}{{N}_{A}}$g | |
| B. | 在常温常压下,11.2LN2含有分子数为0.5NA | |
| C. | 18g水所含有的氢原子数目为2NA,氧原子数目为NA | |
| D. | 1L 0.1mol•L-1K2SO4溶液中,K+ 和SO42-的离子总数是0.3NA |
分析 A、1mol 12C原子中含NA个12C;
B、常温常压下,气体摩尔体积大于22.4L/mol;
C、求出水的物质的量,然后根据1mol水中含2mol氢原子和1mol氧原子来分析;
D、求出硫酸钾的物质的量,然后根据1mol硫酸钾中含2mol钾离子和1mol硫酸根来分析;
解答 解:A、1mol 12C原子中含NA个12C,故1个12C的质量为m=$\frac{12g}{{N}_{A}}$=$\frac{12}{{N}_{A}}$g,故A正确;
B、常温常压下,气体摩尔体积大于22.4L/mol,故11.2L氮气的物质的量小于0.5mol,则分子数小于0.5NA个,故B错误;
C、18g水的物质的量为1mol,而1mol水中含2mol氢原子和1mol氧原子,即为2NA个氢原子和NA个氧原子,故C正确;
D、溶液中硫酸钾的物质的量n=CV=0.1mol/L×1L=0.1mol,而1mol硫酸钾中含2mol钾离子和1mol硫酸根,故0.1mol硫酸钾中含0.3mol离子即0.3NA个,故D正确.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 2NaOH+H2SO4=Na2SO4+2H2OB | B. | Cl2+H2O=HCl+HClO | ||
| C. | CaO+H2O=C a(OH)2 | D. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
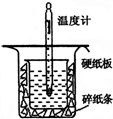 中和热的测定是高中重要的定量实验.取0.55mol/L的NaOH溶液50mL与0.50mol/L的盐酸50mL置于如图所示的装置中进行中和热的测定实验,回答下列问题:
中和热的测定是高中重要的定量实验.取0.55mol/L的NaOH溶液50mL与0.50mol/L的盐酸50mL置于如图所示的装置中进行中和热的测定实验,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 由途径①和②分别制取1molFeCl2,理论上各消耗1molFe,各转移2mole- | |
| B. | 由途径③和④分别制取1 mol Na2SO4,理论上各消耗1 molCl2,各转移2mole- | |
| C. | 由途径⑤和⑥分别制取1 mol H2SO4,理论上各消耗1molS,各转移6mole- | |
| D. | 以上说法都不正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用胶头滴管取少量液体试剂 | B. | 用纸槽向试管底部加入粉未状药品 | ||
| C. | 用燃着的酒精灯点燃另一盞酒精灯 | D. | 用排水法收集难溶于水的气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 用广泛pH试纸测得饱和氯水的pH约为2.2 | |
| B. | 用量筒量取7.60 mL 0.1 mol•L-1盐酸 | |
| C. | 用图1所示的操作可检查装置的气密性 | |
| D. | 实验室用图2所示的装置制取少量的NO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①和②产物的阴阳离子个数比不相等 | |
| B. | ①和②生成等物质的量的产物时,转移电子数不同 | |
| C. | 常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 | |
| D. | 反应:Na2O2(s)+2 Na(s)=2Na2O(s)△H=-317kJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com