
| 微粒 | X | Y | Na+ | A- |
| 浓度/(mol•L-1) | 8.00×10-4 | 2.50×10-10 | 0.100 | 9.92×10-2 |
| A. | 0.1mol•L-1HA溶液的pH=1 | B. | 该温度下Kw=1.0×10-14 | ||
| C. | 微粒X表示OH-,Y表示H+ | D. | 混合溶液中:n(A-)+n(X)=n(Na+) |
分析 某温度下,0.200mol•L-1的HA溶液与0.200mol•L-1的NaOH溶液等体积混合后,溶质为NaA,根据表中数据可知:c( Na+)=0.100mol/L>c(A-)=9.92×10-2mol/L,则HA为弱酸;根据物料守恒可知:c( Na+)=c(A-)+c(HA)=0.100mol/L,则c(HA)=0.100mol/L-9.92×10-2mol/L=8.00×10-4mol/L,故X为HA;根据电荷守恒可知c(OH-)>c(H+),则Y表示H+,据此进行解答.
解答 解:某温度下,0.200mol•L-1的HA溶液与0.200mol•L-1的NaOH溶液等体积混合后,溶质为NaA,根据表中数据可知:c( Na+)=0.100mol/L>c(A-)=9.92×10-2mol/L,则HA为弱酸;根据物料守恒可知:c( Na+)=c(A-)+c(HA)=0.100mol/L,则c(HA)=0.100mol/L-9.92×10-2mol/L=8.00×10-4mol/L,故X为HA;根据电荷守恒可知c(OH-)>c(H+),则Y表示H+,
A.由于HA为弱酸,则0.1mol/L的HA溶液中氢离子浓度小于0.1mol/L,溶液的pH>1,故A错误;
B.温度未知,无法判断该温度下水的离子积,故B错误;
C.根据分析可知,X表示HA,Y表示H+,故C错误;
D.X为HA,则根据物料守恒可知:n(A-)+n(X)=n(Na+),故D正确;
故选D.
点评 本题考查了酸碱混合的定性判断及溶液pH的计算,题目难度中等,明确盐的水解原理、弱电解质的电离平衡为解答关键,注意掌握溶液酸碱性与溶液pH的关系,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:解答题
| 实验操作 | 预期现象与结论 |
| 步骤1: | 有白色沉淀生成,证明待测液中含SO42- |
| 步骤2: | 溶液呈橙黄色,证明待测液中含Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C | B. | HNO3 | C. | CO2 | D. | SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
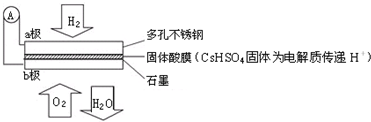
| A. | 电子通过外电路从a极流向b极 | |
| B. | H+由a极通过固体酸电解质传递到b极 | |
| C. | 电池工作时每转移0.1 mol电子,消耗1.12 LH2 | |
| D. | b极上的电极反应式为:O2+4H++4e-=2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
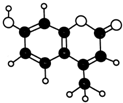
| A. | 分子式为C11H9O3 | B. | 不能使溴水褪色 | ||
| C. | 属于芳香族化合物 | D. | 不能与Na0H溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
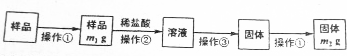
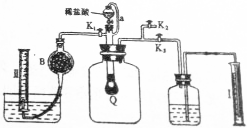
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
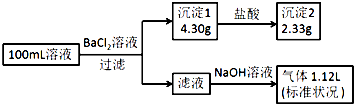 某100mL溶液可能含有Na+、NH4+、Fe3+、CO32-、SO42-、Cl-中的若干种,取该溶液进行连续实验,实验过程如图:(所加试剂均过量,气体全部逸出)下列说法不正确的是( )
某100mL溶液可能含有Na+、NH4+、Fe3+、CO32-、SO42-、Cl-中的若干种,取该溶液进行连续实验,实验过程如图:(所加试剂均过量,气体全部逸出)下列说法不正确的是( )| A. | 原溶液一定存在CO32-和SO42-,一定不存在Fe3+ | |
| B. | 原溶液一定存在Cl-,可能存在Na+ | |
| C. | 原溶液中c(Cl-)≥0.1mol•L-1 | |
| D. | 若原溶液中不存在Na+,则c(Cl-)<0.1mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com