
【题目】阿司匹林(主要成分为乙酰水杨酸)是解热止痛、治疗感冒的药物.它是由水杨酸(邻羟基苯甲酸)与醋酸酐进行酯化反应制得的.其反应原理如下: 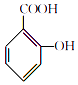 +
+ ![]()
![]()
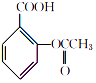 +CH3COOH
+CH3COOH
为避免醋酸酐水解,所用原料、仪器要充分干燥.有关物质的参数如表:
名称 | 式量 | 性质 | 熔点/℃ | 沸点/℃ | 溶解度 | ||
水 | 乙醇 | 乙酸乙酯 | |||||
水杨酸 | 138 | 白色结晶粉末、无臭 | 157~159 | 211 | 溶 | 易溶 | 易溶 |
醋酸酐 | 102 | 无色液体、易燃、有醋酸味 | ﹣73.1 | 138.6 | 易溶 | 溶 | 易溶 |
乙酸水杨酸 | 180 | 白色针状结晶 | 135 | 321.4 | 冰水微溶、热水可溶 | 易溶 | 微溶 |
制取阿司匹林的工艺流程如下:
回答下列问题:
(1)浓磷酸的作用是 . 步骤②的加热方式为水浴加热,温度控制在℃.
(2)向粗产物中加入乙酸乙酯的作用是 .
(3)验证最后得到的乙酰水杨酸产品较为纯净的方法是 .
(4)精制后乙酰水杨酸的质量为8.91g,则其产率为 , 造成产率低的原因可能有(任写一点).
【答案】
(1)催化剂;75~80
(2)溶解水杨酸和醋酸酐等杂质,同时减少乙酰水杨酸因溶解而造成的损失
(3)测定产品熔点
(4)66%;反应温度没有控制好(或粗产品回流时的温度过高,造成产品水解发生副反应等)
【解析】解:(1)浓磷酸作催化剂;由反应可知步骤②的加热方式为水浴加热,温度在75~80℃; 所以答案是:催化剂;75~80;(2)由表可知乙酸乙酯可溶解水杨酸和醋酸酐等杂质,乙酰水杨酸微溶于乙酸乙酯,同时减少乙酰水杨酸因溶解而造成的损失;
所以答案是:溶解水杨酸和醋酸酐等杂质,同时减少乙酰水杨酸因溶解而造成的损失;(3)测定产品熔点与恒定熔点比较可以验证最后得到的乙酰水杨酸产品较为纯净;
所以答案是:测定产品熔点;(4)0.075mol水杨酸与0.265mol醋酸酐反应,由于醋酸酐的物质的量大于水杨酸,所以得到的乙酰水杨酸应该按照水杨酸来计算,故理论上得到乙酰水杨酸的质量为0.075mol×180g/mol=13.5g,所以乙酰水杨酸的产率为(8.91g÷13.5g)×100%=66%,反应温度没有控制好、粗产品回流时的温度过高,造成产品水解发生副反应等造成产率低;
所以答案是:66%;反应温度没有控制好(或粗产品回流时的温度过高,造成产品水解发生副反应等).


科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的值,下列叙述正确的是( )
A.含有NA个氦原子的氦气在标准状况下的体积约为11.2L
B.常温常压下,44g CO2含有的原子数为3NA
C.常温常压下,11.2L氧气所含的原子数为NA
D.标准状况下,11.2L H2O 含有的分子数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除杂质(括号中物质为杂质)所用试剂或方法不正确的是( )
A.CO2(CO):O2
B.MgO(Al2O3):NaOH溶液
C.NaHCO3溶液(Na2CO3):过量的CO2
D.CO2(HCl):饱和NaHCO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按下图装置,持续通入气体X,可看到a处有红色物质生成,b处变蓝,c处得到液体,则气体X可能是( )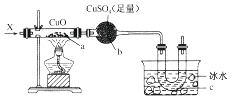
A.H2
B.CO和H2
C.NH3
D.CH3CH2OH(蒸气)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N和Si是合成新型非金属材料的两种重要元素.请回答:
(1)基态Si原子的价层电子排布图为;其2p能级的轨道有个伸展方向,电子云的形状为 .
(2)Si原子可形成多种氢化物,其中Si2H4中Si原子的价层电子对数目为 , Si原子的杂化轨道类型为 .
(3)N和Si形成的原子晶体中,N原子的配位数为 .
(4)NaN3常作为汽车安全气囊的填充物,其焰色反应为黄色.大多数金属元素有焰色反应的微观原因为;N3﹣中σ键和π键的数之比为 . B、F与N三种元素同周期,三种基态原子的第一电离能由大到小的顺序为(用元素符号表示).
(5)NaNO2是一种重要的工业原料,NO2﹣的空间构型为 .
(6)SiO2的晶胞与金刚石(如图所示)相似,可以看作Si原子替代C原子后,在两个成键的Si原子间插入1个O原子形成. 
则:①晶胞中最小的环含有个原子.
②若晶体密度为ρgcm﹣3 , 阿伏伽德罗常数为NA , 晶胞中两个最近的Si原子核之间的距离为pm(用代数式表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用萃取法从碘水中分离出碘,所用萃取剂应具有的性质是( )
①不和碘水发生化学反应 ②能溶于水 ③应是极性溶剂 ④不溶于水 ⑤应是非极性溶剂.
A. ①④⑤B. ①③④C. ①②⑤D. ①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将20g质量分数为14%的KNO3溶液与30g质量分数为24%的KNO3溶液混合,得到的密度为1.26 g/mL的混合溶液.计算:
(1)混合后溶液的质量分数.
(2)混合后溶液的物质的量浓度.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,正确的是 ( )
A. 12g碳所含的原子数就是阿伏加德罗常数
B. 阿伏加德罗常数没有单位
C. “物质的量”指物质的质量
D. 摩尔是表示物质的量的单位,每摩尔物质含有阿伏加德罗常数个微粒
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com