
| A. | 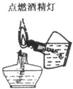 | B. | 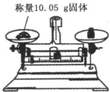 | C. | 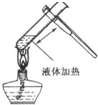 | D. | 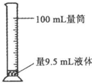 |
分析 A.不能用燃着的酒精灯引燃另一只酒精灯;
B.托盘天平的感量为0.1g;
C.加热试管时,试管中液体不能超过容积的$\frac{1}{3}$,试管夹在试管口上方,试管倾斜45℃,不对着自己或别人;
D.量筒的规格和液体体积接近,减少误差.
解答 解:A.不能用燃着的酒精灯引燃另一只酒精灯,应火柴点燃,故A错误;
B.托盘天平的感量为0.1g,应称量10.1g,故B错误;
C.加热试管时,试管中液体不能超过容积的$\frac{1}{3}$,试管夹在试管口上方,试管倾斜45℃,不对着自己或别人,操作合理,故C正确;
D.量筒的规格和液体体积接近,减少误差,应选10mL量筒,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握实验基本操作、实验安全为解答的关键,侧重分析与实验能力的考查,注意实验评价性分析,题目难度不大.


科目:高中化学 来源: 题型:多选题
| A. | 0.20 | B. | 0.16 | C. | 0.12 | D. | 0.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 裂化汽油不能萃取溴水中的溴 | |
| B. | 石油的分馏以及煤的气化和液化是物理变化 | |
| C. | 煤中含有大量的苯等芳香烃,煤是芳香烃的主要来源 | |
| D. | 煤属于有机化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 定容时仰视液面 | |
| B. | 溶解后立即转移到容量瓶中 | |
| C. | 未洗涤烧杯和玻璃棒 | |
| D. | 溶液配好摇匀后,发现液面低于刻度线,又加水至液面与刻度线相切 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
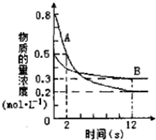 某温度下,在2L密闭容器中投入一定量的A、B发生反应:3A(g)+bB (g)?cC(g)△H=-Q kJ•mol-1(Q>0).12s 时达到平衡,生成C的物质的量为0.8mol,反应过程如图所示.下列说法正确的是( )
某温度下,在2L密闭容器中投入一定量的A、B发生反应:3A(g)+bB (g)?cC(g)△H=-Q kJ•mol-1(Q>0).12s 时达到平衡,生成C的物质的量为0.8mol,反应过程如图所示.下列说法正确的是( )| A. | 前12s内,A的平均反应速率为0.025mol•L-1•s-1 | |
| B. | 12s后,A的消耗速率等于B的生成速率 | |
| C. | 化学计量数之比b:c=1:2 | |
| D. | 12s内,A和B反应放出的热量为0.2Q kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
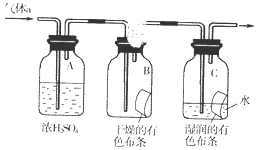 氯气是一种化学性质活泼的非金属单质,工业上可用氯气制取漂白粉、有机溶剂等.
氯气是一种化学性质活泼的非金属单质,工业上可用氯气制取漂白粉、有机溶剂等.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com