
【题目】常温下,pH=1的某溶液A中含有NH4+、K+、Na+、Fe3+、Al3+、Fe2+、CO32-、NO3-、Cl-、I-、SO42-中的4种,且溶液中各离子的物质的量浓度均为0.1mol/L,现取该溶液进行有关实验,实验结果如下图所示: 下列有关说法正确的是

A.该溶液中一定有上述离子中的NO3-、Al3+、SO42-、Cl-四种离子
B.实验消耗Cu 14.4g,则生成气体丁的体积为3.36L
C.沉淀乙一定有BaCO3,可能有BaSO4
D.一定没有Fe3+,但是无法确定是否含有I-
【答案】A
【解析】
试题分析:pH=1,说明溶液显强酸性,说明有H+,CO32-一定不存在,A、溶液A中加入过量的(NH4)2CO3溶液,Fe3+和CO32-发生双水解,生成氢氧化铁沉淀(红褐色),说明原溶液中不含Fe3+,但溶液乙中加入Cu和硫酸,产生气体丙,气体丙遇空气变成红棕色气体丁因此,丁为NO2,丙为:NO,说明原溶液中有NO3-,但是NO3-在酸性条件下具有氧化性,因为Fe2+、I-具有还原性,因此不能大量存在,因此白色沉淀甲为Al(OH)3,原溶液中含有Al3+,根据溶液显电中性,阳离子所带的电荷数总物质的量浓度为3n(Al3+)+n(H+)=3×0.1+0.1=0.4mol·L-1,而NO3-所带电荷数为0.1mol·L-1,又因为各离子浓度为0.1mol·L-1,因此原溶液中含有SO42-、Cl-,故正确;B、题目中没有说标准状况,因此无法计算气体体积,故错误;C、因为加的是过量的(NH4)2CO3,所以有Ba2++CO32-=BaCO3↓,根据A选项的分析,原溶液中有SO42-,因此也就有Ba2++SO42-=BaSO4↓,因此沉淀乙一定是BaCO3、BaSO4,故错误;D、根据A选项的分析,原溶液中一定没有I-,故错误。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列示意图与对应的反应情况正确的是( )
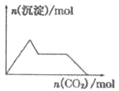
A. 含0.0l mol KOH和0.01 mol Ca(OH)2的混合溶液中缓慢通入CO2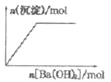
B. NaHSO4溶液中逐滴加入Ba(OH)2溶液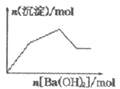
C. KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液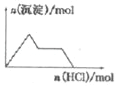
D. NaAlO2溶液中逐滴加入盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制500 mL0.5 mol·L-1的NaOH溶液,试回答下列问题:
(1)计算:需要NaOH固体的质量为____________。(精确到0.1g)
(2)有以下仪器:①烧杯 ②100ml量筒 ③1000ml容量瓶 ④500mL容量瓶 ⑤玻璃棒 ⑥托盘天平(带砝码) ⑦滴定管
(Ⅰ)配制时,必须使用的仪器有_____(填代号),还缺少的仪器是__;
(Ⅱ)实验两次用到玻璃棒,其作用分别是:______________、_____________。
(Ⅲ)配制时,一般可分为以下几个步骤:①称量②计算③溶解④摇匀⑤转移⑥洗涤⑦定容⑧冷却。其正确的操作顺序为_______________
(3)某学生实际配制NaOH溶液的浓度为0.48 mol·L-1,原因可能是_______。
A.使用滤纸称量氢氧化钠固体
B.容量瓶中原来存有少量蒸馏水
C.溶解后的烧杯未经多次洗涤
D.胶头滴管加水定容时俯视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】)常温下钛的化学活性很小,在较高温度下可与多种物质反应。
(1)工业上由金红石(含TiO2大于96%)为原料生产钛的流程如下:

① 沸腾氯化炉中发生的主要反应为:_____________。
② 己知:Ti (s)+2Cl2(g)=TiCl4(l) △H=akJ/mol;
2Na(s)+Cl2(g)=2NaCl(s) △H=bkJ/mol;
Na(s) = Na (l) △H=ckJ/mol
则TiCl4(l)+4Na(l)=Ti(s)+4NaCl(s) △H=________kJ/mol
③ TiCl4遇水强烈水解,写出其水解的化学方程式________。
(2)TiO2直接电解法生产钛是一种较先进的方法,电解质为熔融的氯化钙,原理如图所示。二氧化钛电极连接电源_____极,该极电极反应为__________。

(3)若以二甲醚(CH3OCH3)、空气、氢氧化钾溶液为原料,多孔石墨为电极构成的燃料电池提供上述电解的电源,则该电池工作时负极的电极反应式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 14C和l2C互称为同位素 B. 苯和环乙烷互称为同分异构体
C. 丁烷与戊烷互称为同系物 D. 金刚石和石墨称为同素异形体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把V L含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为 ( )
A. ![]() mol·L-1 B.
mol·L-1 B. ![]() mol·L-1
mol·L-1
C. ![]() mol·L-1 D.
mol·L-1 D. ![]() mol·L-1
mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①Fe2O3(s)+3C(s) ===2Fe(s)+3CO(g) ΔH=+494kJ·mol-1
②CO(g)+1/2O2(g) ===CO2(g) ΔH=-283 kJ·mol-1
③C(s)+1/2O2(g)===CO(g) ΔH=-110kJ·mol-1
则反应Fe2O3(s)+3C(s)+ 3/2O2(g) ===2Fe(s)+3CO2(g)的焓变是
A. -355 kJ B. +355 kJ C. -355 kJ mol-1 D. +355 kJ mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既属于氧化还原反应,又是吸热反应的是( )
A.天然气在空气中燃烧的反应 B.灼热的木炭与CO2的反应
C.铁粉与稀硫酸的反应 D.Ba(OH)2 8H2O晶体与NH4Cl晶体的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工业残渣主要成分为Fe2O3(含有少量FeO、Cu、Mg等杂质)。某课外兴趣小组利用该残渣制取Fe2O3粉末的流程如下:(说明:流程中“向黄色溶液加入MgO”的目的是调节溶液的酸碱性,使Fe3+生成沉淀而Mg2+不沉淀。)
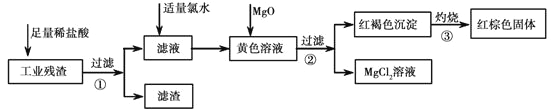
请回答下列问题:
(1)加入足量稀盐酸后,发生化学反应的类型有_____________(填写代号)。
A. 氧化还原反应 B.化合反应 C.分解反应 D.复分解反应
(2)加入适量氯水的作用是____________________________.
(3)写出灼烧红褐色沉淀时发生反应的化学方程式_____________________。实验室灼烧红褐色沉淀可选用的装置是__________(填序号)。

(4)若向黄色溶液中加入过滤①后的滤渣,发生反应的离子方程式为___________。
(5)检验黄色溶液中Fe3+是否完全沉淀的方法是:取过滤②后的少量滤液于试管中,____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com