

分析 羟基和苯环直接相连,属于酚类,官能团羟基与链烃基或者苯环侧链的碳原子相连形成的化合物属于醇类;醇、酚中均含-OH,但连接烃基不同;
醚类含C-O-C,结构相似;结构相似,组成相差n个CH2原子团的有机物为同系物,而分子式相同、结构不同的有机物互为同分异构体,以此来解答.
解答 解:上述物质中①⑦含-OH,且不与苯环直接相连,为醇类物质;
③④⑤含-OH,与苯环直接相连,为酚类物质;
②⑥中含C-O-C,为醚类物质,
①与⑦、②与⑥、③与⑤与①为同系物;
②和③、⑤和⑥均符合分子式相同,结构不同,则互为同分异构体,
故答案为:①⑦;③④⑤;②⑥;①与⑦、②与⑥、③与⑤与①;②和③、⑤和⑥.
点评 本题考查有机物的官能团与结构,为高频考点,把握常见有机物的官能团及物质分类为解答的关键,侧重基础知识的考查,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 2H2(g)+O2(g)=2H2O(g)△H=-Q1kJ/mol; 2H2(g)+O2(g)=2H2O(g))△H=-Q2kJ/mol | |
| B. | S(g)+O2(g)=SO2(g)△H=-Q1kJ/mol; S(s)+O2(g)=SO2(g))△H=-Q2kJ/mol | |
| C. | C(s)+$\frac{1}{2}$O2(g)=CO2(g))△H=-Q1kJ/mol; C(s)+O2(g)=CO(g))△H=-Q2kJ/mol | |
| D. | H2(g)+Cl2(g)=2HCl(g)△H=-Q1kJ/mol; $\frac{1}{2}$H2(g)+Cl2(g)=HCl(g))△H=-Q2kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
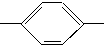 CH═N
CH═N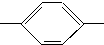 CH2CH2CH2CH3 MBBA
CH2CH2CH2CH3 MBBA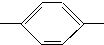 CHO 醛A
CHO 醛A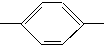 NH2 胺B
NH2 胺B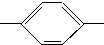 NH2、CH3CH2CH2CH2
NH2、CH3CH2CH2CH2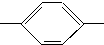 NH2、CH3CH2CH(CH3)
NH2、CH3CH2CH(CH3)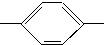 NH2、(CH3)3C
NH2、(CH3)3C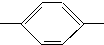 NH2.
NH2.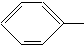 COOCH3、
COOCH3、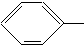 OOCCH3、HCOO
OOCCH3、HCOO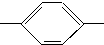 CH3、
CH3、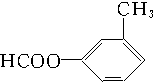 、
、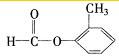 、
、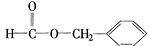 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
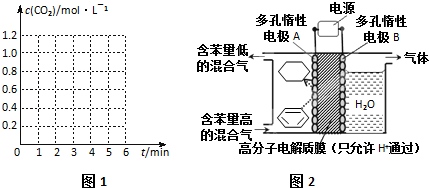
| 实验编号 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | |
| H2O | CO | CO2 | |||
| 1 | 500 | 4 | 8 | 3.2 | 4 |
| 2 | 750 | 2 | 4 | 0.8 | 3 |
| 3 | 750 | 2 | 4 | 0.8 | 1 |
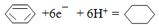 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
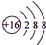 .
. .常温下,D2E2是一种橙黄色的液体,遇水易水解,并产生能使品红褪色的气体.下列说法中正确的是ACD.
.常温下,D2E2是一种橙黄色的液体,遇水易水解,并产生能使品红褪色的气体.下列说法中正确的是ACD.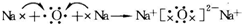 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ①②③ | C. | ②④ | D. | ①③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由Cl2+H2O=HCl+HClO可推出F2+H2O=HF+HFO | |
| B. | HCl的水溶液是强酸,推出HF水溶液也是强酸 | |
| C. | 由2Fe+3Cl2=2FeCl3可推出2Fe+3I2=2FeI3 | |
| D. | Na、K在属于同一主族,化学性质相似,Na常温下与水剧烈反应,故K常温下也能与水剧烈反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com