大气中硫、氮的氧化物是形成酸雨的主要物质.某地酸雨中可能含有下列离子:Na
+、Ba
2+、NH
4+、Al
3+、Cl
-、SO
32-、SO
42-、NO
3-等.某研究小组取该地一定量的酸雨,浓缩后将所得澄清试液分成3份,进行如下实验:
| 试样 |
所加试剂 |
实验现象 |
| 第一份试液 |
滴加适量的淀粉KI溶液 |
呈蓝色 |
| 第二份试液 |
滴加用盐酸酸化的BaCl2溶液 |
有白色沉淀 |
| 第三份试液 |
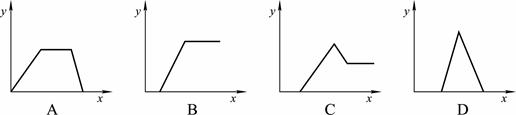
滴加NaOH溶液,加热,加入的NaOH溶液体积(V)与生成的沉淀、产生的气体(n)的关系如图 |
|
请回答下列问题:
(1)根据实验结果判断该酸雨中肯定不存在的离子是
SO32-、Ba2+
SO32-、Ba2+
,不能确定的离子有
Na+、Cl-
Na+、Cl-
.
(2)写出试液中滴加淀粉KI溶液时发生反应的离子方程式:
6I-+2NO3-+8H+=2NO↑+3I2+4H2O
6I-+2NO3-+8H+=2NO↑+3I2+4H2O
.
(3)第三份试液滴加NaOH溶液,加热整个过程中有多个反应,写出其中两个反应的离子方程式
OH
-+H
+=H
2O,NH
4++OH
-NH
3↑+H
2O
OH
-+H
+=H
2O,NH
4++OH
-NH
3↑+H
2O
、
Al3++3OH-=Al(OH)3↓,Al(OH)3+OH-=AlO2-+2H2O
Al3++3OH-=Al(OH)3↓,Al(OH)3+OH-=AlO2-+2H2O
.
(4)设计实验方案,检验该中是否存在Cl
-:
少量试液滴加足量的Ba(NO3)2溶液,静置取上层澄清液加HNO3酸化的AgNO3溶液,若有白色沉淀生成,则证明存在Cl-
少量试液滴加足量的Ba(NO3)2溶液,静置取上层澄清液加HNO3酸化的AgNO3溶液,若有白色沉淀生成,则证明存在Cl-
.
(5)该小组为了探究NO参与硫酸型酸雨的形成过程,在烧瓶中充入含有少量NO的SO
2气体,再慢慢通入O
2,发生化学反应后,再喷洒适量蒸馏水即得硫酸型酸雨,则NO在上述反应中的作用是
催化剂
催化剂
.

 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 如图所示为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
如图所示为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
 下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:




 或
或
 或
或

 4Al+3O2↑
4Al+3O2↑ 4Al+3O2↑
4Al+3O2↑ 或
或
 或
或

