
【题目】室温条件下,下列有关电解质溶液的描述正确的是
A.等浓度的KHSO3溶液与KOH溶液等体积混合:c(OH)c(H+)=c(![]() ) + c(H2SO3)
) + c(H2SO3)
B.pH相同的氨水和Ba(OH)2溶液中:2c(![]() )= c(Ba2+)
)= c(Ba2+)
C.等浓度的Na2SO4溶液与NH4Cl溶液等体积混合:c(Na+) +c(![]() )+c(NH3·H2O)=2c(
)+c(NH3·H2O)=2c(![]() ) +c(Cl)
) +c(Cl)
D.1 L 0.1 mol·L1的KAl(SO4)2·12H2O溶液中:c(K+)+c(Al3+)+c(H+)=c(OH)+c(![]() )
)
【答案】C
【解析】等浓度的KHSO3溶液与KOH溶液等体积混合相当于K2SO3溶液,该溶液中存在电荷守恒,即c(K+)+c(H+)=2c(![]() )+ c(
)+ c(![]() )+c(OH),还存在物料守恒,即c(K+)=2c(
)+c(OH),还存在物料守恒,即c(K+)=2c(![]() )+2c(
)+2c(![]() )+
)+
2c(H2SO3),两个等式联立消去c(K+),可得c(OH)c(H+)=c(![]() ) + 2c(H2SO3),A项错误;氨水中,根据电荷守恒,c(
) + 2c(H2SO3),A项错误;氨水中,根据电荷守恒,c(![]() )=c(OH) c(H+),Ba(OH)2溶液中,根据电荷守恒,2c(Ba2+)= c(OH) c(H+),pH相同的氨水和Ba(OH)2溶液中c(OH) c(H+)相等,则c(
)=c(OH) c(H+),Ba(OH)2溶液中,根据电荷守恒,2c(Ba2+)= c(OH) c(H+),pH相同的氨水和Ba(OH)2溶液中c(OH) c(H+)相等,则c(![]() )= 2c(Ba2+),B项错误;Na2SO4溶液存在:c(Na+)=2c(
)= 2c(Ba2+),B项错误;Na2SO4溶液存在:c(Na+)=2c(![]() ),NH4Cl溶液存在:c(
),NH4Cl溶液存在:c(![]() )+c(NH3·H2O)=c(Cl),两个等式相加即得:c(Na+)+c(
)+c(NH3·H2O)=c(Cl),两个等式相加即得:c(Na+)+c(![]() )+
)+
c(NH3·H2O)=2c(![]() )+c(Cl),C项正确;由溶液中的电荷守恒可知KAl(SO4)2·12H2O溶液中:c(K+)+
)+c(Cl),C项正确;由溶液中的电荷守恒可知KAl(SO4)2·12H2O溶液中:c(K+)+
3c(Al3+)+c(H+)=c(OH)+2c(![]() ),D项错误。
),D项错误。


科目:高中化学 来源: 题型:
【题目】利用如图装置,可以完成许多电化学实验。下列有关此装置的叙述中,正确的是

A.若X为铜棒,Y为硫酸铜溶液,开关K置于N处,铁棒质量将增加,溶液中铜离子浓度将减小
B.若X为碳棒,Y为NaCl溶液,开关K置于N处,可减缓铁的腐蚀,溶液中阳离子向碳棒电极移动
C.若X为碳棒,Y为硫酸铜溶液,开关K置于M处,碳棒质量将增加,此时外电路中的电子向碳电极移动
D.若X为铜棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阳极的阴极保护法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无线电频率可以降低盐水中所含元素之间的“结合力”,释放出氢原子,若点火,氢原子就会在该种频率下持续燃烧。上述中“结合力”实质是
A.分子间作用力B.非极性共价键
C.氢键D.极性共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于强弱电解质及非电解质的组合完全正确的是( )
A | B | C | D | |
强电解质 | NaCl | H2SO4 | NaOH | HNO3 |
弱电解质 | HF | BaSO4 | CaCO3 | CH3COOH |
非电解质 | Cl2 | CO2 | C2H5OH | SO2 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下面的反应路线及所给信息,回答下列问题:
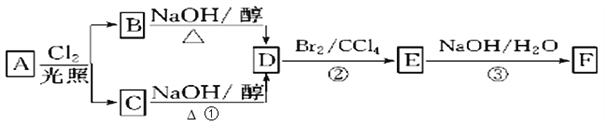
(1)11.2L(标准状况)的烃A在氧气中充分燃烧可以产生88gCO2和45gH2O,A的分子式是________________。
(2)B和C均为一氯代烃,已知C中只有一种等效氢,则B的名称(系统命名)为_______。
(3)D的结构简式_____________, ③的反应类型是 ______________。
(4)写出③的反应化学方程式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池的电池反应为:Fe+2Fe3+ == 3Fe2+,与此电池反应不符的原电池是( )
A. 铜片、铁片、FeCl3溶液组成的原电池
B. 石墨、铁片、Fe(NO3)3溶液组成的原电池
C. 铁片、锌片、Fe2(SO4)3溶液组成的原电池
D. 银片、铁片、Fe(NO3)3溶液组成的原电池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X元素原子的L层比Y元素原子的L层少3个电子,X元素原子的核外电子总数比Y原子核外电子总数少5个,则X、Y可形成的化合物是
A. 离子化合物Y(XO4)2 B. 离子化合物Y2X3
C. 共价化合物XY2 D. 离子化合物Y3X2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别处于第二、第三周期的主族元素A和B,它们的离子电子层结构相差两层,已知A处于第m族,B处于第n族,A只有正化合价,则A、B的原子序数分别是( )
A. m、n B. 3、7 C. m-2、10-n D. m+2、n+10
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com