
| A. | 3v生成(N2)=v生成(H2) | B. | v消耗(N2)=v消耗(NH3)? | ||
| C. | v消耗(N2)=3v生成(H2)? | D. | 2v消耗(H2)=3v消耗(NH3) |
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:解答题
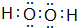 .写出甲的一种用途作高能燃料.
.写出甲的一种用途作高能燃料.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 农村推广建造沼气池,实现了生物质能向热能的转化 | |
| B. | 光-生物质能转换的本质是光-化学能的转换 | |
| C. | 科学家们预言,氢能将成为21世纪的重要能源 | |
| D. | 化石燃料蕴藏的能量来自远古时期生物体所吸收利用的太阳能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeBr2溶液中通入少量的Cl2:2Fe2++Cl2═2Fe3++2Cl- | |
| B. | Ca(HCO3)2溶液与过量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| C. | 等物质的量的MgCl2、Ba(OH)2和HCl溶液混合:Mg2++2OH-═Mg(OH)2↓ | |
| D. | 铜溶于稀硝酸中:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 吸收471kJ能量 | B. | 放出479kJ能量 | C. | 吸收479kJ能量 | D. | 放出445kJ能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 活性炭/mol | NO/mol | A/mol | B/mol | |
| 起始状态 | 2.030 | 0.100 | 0 | 0 |
| 2min时 | 2.000 | 0.040 | 0.030 | 0.030 |
 (4)碳元素可形成数量众多,分布极广的有机化合物,其中甲醇是常见的燃料,甲醇燃料电池的结构示意图如下,一极通入甲醇,另外一极通入氧气;电解质溶液是稀硫酸,电池工作时总反应式:2CH3OH+3O2=2CO2+4H2O.
(4)碳元素可形成数量众多,分布极广的有机化合物,其中甲醇是常见的燃料,甲醇燃料电池的结构示意图如下,一极通入甲醇,另外一极通入氧气;电解质溶液是稀硫酸,电池工作时总反应式:2CH3OH+3O2=2CO2+4H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯与溴水(加成反应) | |
| B. | 苯与浓硝酸(取代反应) | |
| C. | 乙醇与乙酸制乙酸乙酯(酯化反应) | |
| D. | 乙醇在铜、银等催化剂存在下与氧气(取代反应) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
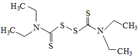 )会抑制肝脏中的乙醛脱氢酶,造成危害,严重的可能导致死亡.许多抗菌药(如:头孢)具有与双硫仑相似的作用,因此服用头孢后严禁饮酒.下列有关说法不正确的是( )
)会抑制肝脏中的乙醛脱氢酶,造成危害,严重的可能导致死亡.许多抗菌药(如:头孢)具有与双硫仑相似的作用,因此服用头孢后严禁饮酒.下列有关说法不正确的是( )| A. | “双硫仑”分子式为C10H12N2S4,在水中的溶解度较小 | |
| B. | 反应①②均属于氧化反应 | |
| C. | 一个人的酒量大小取决于体内上述两种酶的多少 | |
| D. | 乙醛是对人体有害的物质,含官能团名称为“醛基” |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com