
| A. | 1mol铁与1molCl2充分反应,转移电子数为3NA | |
| B. | 常温常压下,2gD216O 中含中子数、质子数、电子数均不相等 | |
| C. | 14g 分子式为CnH2n 的(n≥2)链烃中含有的C=C 的数目一定为$\frac{{N}_{A}}{n}$ | |
| D. | 在含Al3+总数为NA的AlCl3溶液中,Cl-总数为3NA |
分析 A、1mol铁和1mol氯气反应后铁过量;
B、D216O中含有的中子数、质子数和电子数均为10个;
C、CnH2n 的(n≥2)链烃一定为单烯烃;
D、铝离子为弱碱阳离子,在溶液中会水解.
解答 解:A、1mol铁和1mol氯气反应后铁过量,而氯气反应后变为-1价,故1mol氯气转移2mol电子即2NA个,故A错误;
B、D216O中含有的中子数、质子数和电子数均为10个,故2g重水中含有的中子、电子和质子数相同,故B错误;
C、CnH2n 的(n≥2)链烃一定为单烯烃,而14g此烯烃的物质的量为n=$\frac{14g}{14ng/mol}$=$\frac{1}{n}$mol,则含有的碳碳双键的物质的为$\frac{1}{n}mol$,个数为$\frac{{N}_{A}}{n}$个,故C正确;
D、铝离子为弱碱阳离子,在溶液中会水解,故当铝离子为NA个时,溶液中的氯离子的个数大于3NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


 快捷英语周周练系列答案
快捷英语周周练系列答案科目:高中化学 来源: 题型:解答题
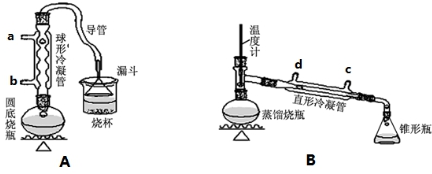
| 物质 | 熔点/℃ | 沸点/℃ |
| 1-丁醇 | -89.5 | 117.3 |
| 1-溴丁烷 | -112.4 | 101.6 |
| 丁醚 | -95.3 | 142.4 |
| 1-丁烯 | -185.3 | -6.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
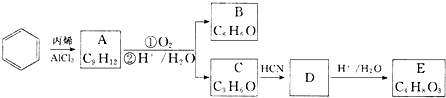
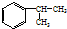 ,A的含有苯环的同分异构体(除A外)有7种.
,A的含有苯环的同分异构体(除A外)有7种.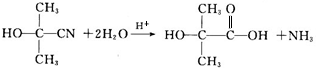 .
.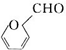 )是一种重要的化工原料,如同甲醛与苯酚反应生成酚醛树脂,它也可与苯酚反应生成糠醛树脂,写出该反应的化学方程式:
)是一种重要的化工原料,如同甲醛与苯酚反应生成酚醛树脂,它也可与苯酚反应生成糠醛树脂,写出该反应的化学方程式: .
. ,G
,G .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
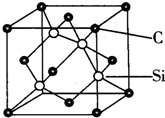 铜、镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料.请回答:
铜、镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料.请回答: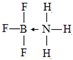 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molCl2中含有Cl2分子的数目为NA | |
| B. | 标准状况下,22.4L水中含有水分子数目为NA | |
| C. | 含有 1molNa2SO4的溶液中含有钠离子数目为NA | |
| D. | 32gO2中含有氧原子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
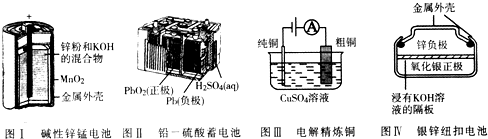
| A. | 图I所示电池中,锌极电极反应为Zn-2e-═Zn2+ | |
| B. | 图Ⅱ所示电池放电过程中,每转移1mo1电子,生成1mol PbSO4 | |
| C. | 图III所示装置工作过程中,电解质溶液中Cu2+浓度始终不变 | |
| D. | 图Ⅳ所示电池中,Ag2O在电池工作过程中被氧化为Ag |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
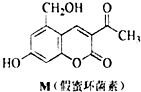
| A. | M的分子式为C12H10O5 | |
| B. | M与Br2只能发生取代反应,不能发生加成反应 | |
| C. | 1 mol M最多能与3mol NaOH反应 | |
| D. | M既能与FeCl3溶液发生反应,也能与CH3COOH发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
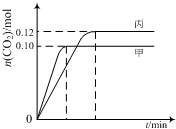 一定温度下,在三个容积均为2.0L的恒容密闭容器中发生反应:2NO(g)+2CO(g)?N2(g)+2CO2(g)
一定温度下,在三个容积均为2.0L的恒容密闭容器中发生反应:2NO(g)+2CO(g)?N2(g)+2CO2(g)| 容器 | 温度/℃ | 起始物质的量/mol | |
| NO (g) | CO (g) | ||
| 甲 | T1 | 0.20 | 0.20 |
| 乙 | T1 | 0.30 | 0.30 |
| 丙 | T2 | 0.20 | 0.20 |
| A. | 该反应的正反应为吸热反应 | |
| B. | 达到平衡时,乙中CO2的体积分数比甲中的小 | |
| C. | T1℃时,若起始时向甲中充入0.40 mol NO、0.40mol CO、0.40mol N2和0.40mol CO2,则反应达到新平衡前v(正)<v(逆) | |
| D. | T2℃时,若起始时向丙中充入0.06mol N2和0.12 mol CO2,则达平衡时N2的转化率大于40% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
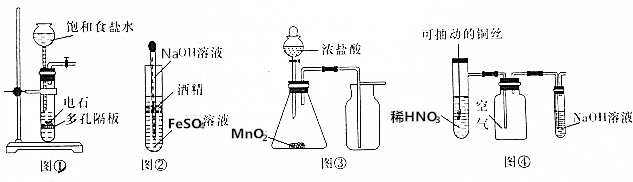
| A. | 用图①所示装置制取少量纯净的乙烯气体 | |
| B. | 用图②所示装置制备Fe(OH)2并能保持长时间观察到白色 | |
| C. | 用图③所示装置制取并收集干燥纯净的Cl2 | |
| D. | 用图④所示装置制取NO并验证其性质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com