
 .
.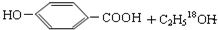 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$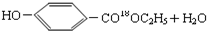 ②E与足量的NaOH溶液反应
②E与足量的NaOH溶液反应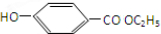 +2NaOH→
+2NaOH→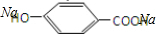 +H2O.
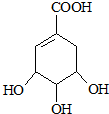
+H2O. 分析 (1)草莽酸含有羟基、碳碳双键、羧基等官能团;
(2)能与氢氧化钠反应的官能团为羧基;
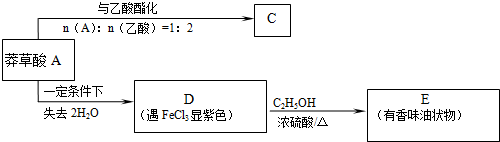
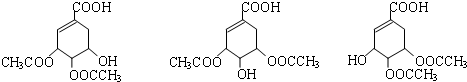
(3)草莽酸含有羟基,可与乙酸发生酯化反应,如与乙酸铵1:2发生酯化反应,可生成三种有机物,C可能为 ,D遇氯化铁变紫色,说明D中含有酚羟基,D的碳环上一氯代物只有两种,应为对称结构,则D可能为
,D遇氯化铁变紫色,说明D中含有酚羟基,D的碳环上一氯代物只有两种,应为对称结构,则D可能为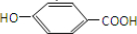 ,E为
,E为 ,以此解答(3)、(4)(5).
,以此解答(3)、(4)(5).
解答 解:(1)由结构简式可知草莽酸含有羟基、碳碳双键、羧基等官能团,故答案为:羟基、碳碳双键、羧基;
(2)能与氢氧化钠反应的官能团为羧基,分子中含有1个羧基,则可与1mol氢氧化钠反应,故答案为:1;
(3)草莽酸含有羟基,可与乙酸发生酯化反应,如与乙酸铵1:2发生酯化反应,可生成三种有机物,C可能为 ,D遇氯化铁变紫色,说明D中含有酚羟基,D的碳环上一氯代物只有两种,应为对称结构,则D可能为
,D遇氯化铁变紫色,说明D中含有酚羟基,D的碳环上一氯代物只有两种,应为对称结构,则D可能为 ,E为
,E为 ,由以上分析可知C可能为
,由以上分析可知C可能为 ,
,
故答案为: ;
;
(4)根据题干推断可知A 到D
到D 的反应为消去反应,故答案为:消去反应;
的反应为消去反应,故答案为:消去反应;
(5)①D→E的反应为酯化反应,反应的方程式为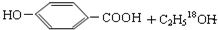 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$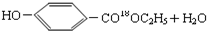 ,
,
故答案为: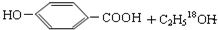 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$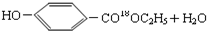 ;
;
②E为 ,与氢氧化钠反应的方程式为
,与氢氧化钠反应的方程式为  +2NaOH→
+2NaOH→ +H2O,
+H2O,
故答案为: +2NaOH→
+2NaOH→ +H2O.
+H2O.
点评 本题考查有机物的合成与推断,侧重于学生的分析能力的考查,为高频考点,注意把握有机物的结构和官能团的性质,为解答该题的关键,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 氮化硅陶瓷--导热剂 | B. | Si和Ge--半导体材料 | ||
| C. | 钢化玻璃--汽车窗玻璃 | D. | SiO2--制光纤 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化铵与八水合氢氧化钡反应 | |
| B. | 碳与水蒸气高温制取水煤气 | |
| C. | 氢氧化钾和硫酸中和 | |
| D. | 碳酸钙高温分解成氧化钙和二氧化碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气溶于水:H2O+Cl2═2H++ClOˉ+Clˉ | |
| B. | 锌片插入稀H2SO4溶液中:Zn+2H+═Zn2++H2↑ | |
| C. | 氢氧化钡溶液与稀硫酸反应:H++SO42-+OH-+Ba2+═H2O+BaSO4↓ | |
| D. | 碳酸钙溶于稀盐酸:CO32-+2H+═H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 CaO2+2HCl.
CaO2+2HCl.| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| CaO2平均生成速率(×10-3mol.s-1) | 7.5 | 8.2 | 9.4 | 8.0 | 7.1 | 6.7 | 5.5 |
 CaO2+2HCl平衡向正方向移动,提高过氧化钙的产量.
CaO2+2HCl平衡向正方向移动,提高过氧化钙的产量. 2CaO(s)+O2(g)△H=2(b-a)kJ•mol-1.
2CaO(s)+O2(g)△H=2(b-a)kJ•mol-1.| 时间/s | n(CaO2)/mol | n(CaO)/mol | n(O2)/mol |
| 0 | 2 | 0 | 0 |
| 1 | 1.4 | 0.6 | 0.3 |
| 2 | 1 | 1 | 0.5 |
| 3 | 1 | 1 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 室温下向1 L pH=1的醋酸溶液中加水,所得溶液的H+数目大于0.1NA | |
| B. | 60g乙酸与足量乙醇发生酯化反应,充分反应后断裂的C-O键数目为NA | |
| C. | 某无水乙醇与足量金属钠反应生成5.6 L H2,该乙醇分子中共价键总数为4 NA | |
| D. | 已知C2H4(g)+H2(g)═C2H6(g)△H=-137.0 kI/mol,乙烯与H2加成时放出68.5 kJ热量,则反应过程中被破坏的碳原子之间共用电子对数目为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com