
| A. | 2A(g)+6B(g)?3C(g)+5D(g) | B. | 3A(g)+B(g)?2C(g)+2D(g) | C. | 3A(g)+B(g)?C(g)+D(g) | D. | A(g)+3B(g)?3C(g)+3D(g) |
分析 利用速率之比等于化学计量数之比、浓度变化量之比等于化学计量数之比,确定m、n、p的关系,平衡后,若保持温度不变,给体系加压,平衡不移动,故反应前后气体的物质的量不变,据此确定q,进而确定m、n、p、q关系,据此判断.
解答 解:A的浓度减少了n mol•L-1,C的浓度增加了$\frac{2}{3}$ n mol•L-1,则m:p=n mol/L:$\frac{2}{3}$ n mol/L=3:2,
平均反应速率vc=2vB,故v(C):v(B):v(C)=n:p=1:2,故m:n:p=3:1:2,
平衡后,若保持温度不变,给体系加压,平衡不移动,故反应前后气体的物质的量不变,即m+n=p+q,
故3+1=2+q,故q=2,所以m:n:p:q=3:1:2:2,
故选B.
点评 本题考查化学反应速率的有关计算、化学平衡移动影响等,难度不大,明确速率之比=化学计量数之比=浓度变化量之比=物质的量变化量之比,判断反应前后气体的物质的量不变是解题关键.


 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
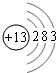 ;
; ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铁溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O | |
| B. | 硫酸铜溶液显酸性:Cu2++2H2O=Cu(OH)2↓+2H+ | |
| C. | 向碳酸氢铵溶液中加过量澄清石灰水:HCO3-+Ca2++OH-=CaCO3↓+H2O | |
| D. | 用酸化的高锰酸钾溶液氧化双氧水:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水中,c(H+)•c(OH-)=1×10-14 | |
| B. | 纯水或水溶液中25℃时,c(H+)•c(OH-)=1×10-14 | |
| C. | NaOH溶液在25℃时,c(H+)•c(OH-)>1×10-14 | |
| D. | 溶液浓度改变或酸碱度改变,Kw随之改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯是无色且带有特殊气味的液体 | |
| B. | 常温下苯是一种不溶于水且密度小于水的液体 | |
| C. | 苯在一定条件下能与溴发生取代反应 | |
| D. | 苯分子中不含碳碳双键,不可能发生加成反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com