
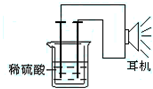
 ���������л�ʵ�����г��õ���Ʒ������������ԭ��Ӧ֪ʶ�͵�ѧ֪ʶ���Լ��������һ��ԭ��أ�����д���пհף�
���������л�ʵ�����г��õ���Ʒ������������ԭ��Ӧ֪ʶ�͵�ѧ֪ʶ���Լ��������һ��ԭ��أ�����д���пհף�

 Сѧ�̲���ȫ���ϵ�д�
Сѧ�̲���ȫ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����֪MgCO3��Ksp=6.82��10-6�������к��й���MgCO3����Һ�У�����c��Mg2+��=c��CO32-������c��Mg2+��?c��CO32-��=6.82��10-6 | ||||
B����֪һ���¶��£�������Һ�����ʵ���Ũ��Ϊc�������Ϊ����Ka=
| ||||
| C�������£���0.10 mol?L-1��NH3?H2O��Һ�м�������NH4Cl���壬��ʹNH3?H2O�ĵ���̶ȼ�������Һ��pH��С | ||||
D������ʱ��M��OH��2��s��?M2+��aq��+2OH-��aq�� Ksp=a c��M2+��=b mol?L-1ʱ����Һ��pH����14+
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 2 |
| A��Q1=Q2=98.32 |
| B��Q1��Q2��98.32 |
| C��Q2��Q1��98.32 |
| D��Q1��Q2��98.32 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
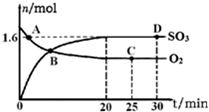 ��Ļ������������Ϳ����з�������Ҫ���ã�
��Ļ������������Ϳ����з�������Ҫ���ã��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com