
【题目】下列叙述中正确的个数有( )
①氧原子的电子排布图:![]() 最外层违背了泡利原理
最外层违背了泡利原理
②处于最低能量状态原子叫基态原子,1s22s22px1→1s22s22py1过程中形成的是发射光谱
③所有元素中,氟的第一电离能最大
④具有相同核外电子排布的粒子,化学性质相同
⑤NCl3中N-Cl键的键长比CCl4中C-Cl键的键长短
⑥金属元素的电负性均小于2
⑦主族元素的电负性越大,其元素原子的第一电离能一定越大
⑧在任何情况下,都是σ键比π键强度大
A.0个B.1个C.2个D.3个
【答案】B
【解析】
①泡利不相容原理又称泡利原理,是指确定的一个原子轨道上最多可容纳两个电子,而这两个电子的自旋方向必须相反,同时要遵循洪特规则,即电子分布到原子轨道时,优先以自旋相同的方式分别占据不同的轨道,因为这种排布方式原子的总能量最低。则氧原子的电子排布图:![]() 最外层违背了洪特规则,故①正确;
最外层违背了洪特规则,故①正确;
②处于最低能量状态原子叫基态原子,处于高能级的原子或分子在向较低能级跃迁时产生辐射,将多余的能量发射出去形成的光谱叫发射光谱,1s22s22px1→1s22s22py1过程中,由于p能级有三个相同的轨道,能量大小相同,即px = py = pz,不能形成的发射光谱,故②错误;
③稀有气体的原子结构是稳定结构,同周期稀有气体的第一电离能最大,同族自上而下第一电离能降低,故氦元素的第一电离能最大,故③错误;
④两种粒子,核外电子排布相同则化学性质相似,也可能相差较大,如Ne与Na+,故④错误;
⑤因为C的原子半径比N的原子半径大,所以 CCl4中C—Cl键键长比NCl3中N—Cl键键长长,故⑤错误;
⑥一般金属元素的电负性小于2.0,非金属元素的电负性大于2.0,但两者之间没有严格的界限,不能把电负性2.0作为划分金属和非金属的绝对标准,故⑥错误;
⑦主族元素原子的第一电离能、电负性变化趋势基本相同,但电离能变化有特例,如电负性:O>N,但第一电离能:O<N,故⑦错误;
⑧σ键不一定比π键强度大,如氮气中σ键的强度比π键强度小,故⑧错误;
综上,正确的有①1个;
答案选B。


科目:高中化学 来源: 题型:
【题目】下列依据热化学方程式得出的结论正确的是( )
A.已知C(石墨,s) = C(金刚石,s) ΔH>0,则金刚石比石墨稳定
B.已知2SO2(g)+O2(g) ![]() 2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量
2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量
C.已知H+(aq)+OH-(aq) = H2O(l) ΔH=-57.3kJ·mol-1,则任何酸碱中和反应的热效应数值均为57.3kJ
D.已知2C(s)+2O2(g) = 2CO2(g) ΔH1, 2C(s)+O2(g)=2CO(g) ΔH2,则ΔH1<ΔH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用标准浓度的氢氧化钠溶液来滴定未知浓度的盐酸,下列操作中会使盐酸测定的浓度偏大的是( )
①酸式滴定管用蒸馏水洗净后,未用盐酸润洗
②锥形瓶中盛有少量蒸馏水,再加待测液
③碱式滴定用蒸馏水洗净后,未用标准溶液润洗
④滴定前碱式滴定管尖端气泡未排除,滴定后气泡消失
⑤滴定后观察碱式滴定管读数时,视线高于刻度线
A.①④B.①③C.②⑤D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某同学设计的原电池装置,下列叙述中正确的是( )

A.电极Ⅰ上发生还原反应,作原电池的负极
B.盐桥中装有含氯化钾的琼脂,其作用是传递电子
C.该原电池的总反应为: Fe3++Cu=Cu2++Fe2+
D.电极Ⅱ的电极反应式为:Cu-2e-=Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在t ℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。又知t ℃时AgCl的Ksp=4×10-10 mol2·L-2,下列说法不正确的是( )

A.在t ℃时,AgBr的Ksp为4.9×10-13 mol2·L-2
B.在AgBr饱和溶液中加入NaBr固体,可使溶液由c点到b点
C.图中a点对应的是AgBr的不饱和溶液
D.在t ℃时,AgCl(s)+Br-(aq)![]() AgBr(s)+Cl-(aq)的平衡常数K≈816
AgBr(s)+Cl-(aq)的平衡常数K≈816
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,在H3PO4溶液中滴入NaOH溶液,溶液中H3PO4、H2PO4-、HPO42-、PO43-的物质的量分数δ(X),δ(X)随pH的变化如图所示。下列叙述错误的是( )

A.Ka2(H3PO4)的数量级为10-8
B.Kh(HPO42-)=1.0×10-6.8
C.pH=7时c(H2PO4-)>c(HPO42-)
D.NaH2PO4溶液显碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯氧化铁是现代电子工业的重要材料.以下是用硫酸厂产生的烧渣![]() 主要成分为
主要成分为![]() 、
、![]() 、FeO、
、FeO、![]() 为原料制备高纯氧化铁
为原料制备高纯氧化铁![]() 软磁
软磁![]() 的生产流程示意图,下列说法不正确的是
的生产流程示意图,下列说法不正确的是![]()
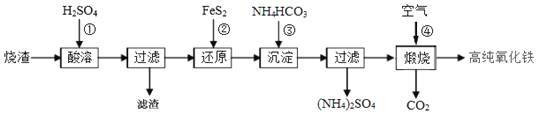
A.酸浸时,常需将烧渣粉碎、并加入过量![]() ,其目的是提铁元素的浸出率,同时抑制铁离子的水解
,其目的是提铁元素的浸出率,同时抑制铁离子的水解
B.加入![]() 时,发生反应
时,发生反应![]() 的离子方程式为
的离子方程式为![]()
C.加入![]() 为了生成
为了生成![]() ,检验
,检验![]() 是否洗涤干净的方法是取最后一次洗涤液少量放入试管,滴加盐酸酸化的氯化钡溶液,若无沉淀生成,说明洗涤干净
是否洗涤干净的方法是取最后一次洗涤液少量放入试管,滴加盐酸酸化的氯化钡溶液,若无沉淀生成,说明洗涤干净
D.煅烧时空气中的氧气作氧化剂,所以用氯气代替空气也可得到高纯氧化铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.2 mol·L-1的一元酸HA与等浓度NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是( )
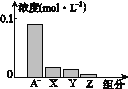
A. HA为强酸
B. 该混合溶液pH=7.0
C. 该混合溶液中:c(A-)+c(Y)=c(Na+)
D. 图中X表示HA,Y表示OH-,Z表示H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】归纳法是髙中化学学习常用的方法之一,某化学研究性学习小组在学习了《化学反应原理》后作出了如下的归纳总结:(均在常温下)
①pH=1的强酸溶液,加水稀释后,溶液中离子浓度都降低
②pH=2的盐酸和pH=l的盐酸,c(H+)之比为2:1
③pH相等的三种溶液:a.CH3COONa b.NaHCO3 c.NaOH,其溶质物质的量浓度由小到大顺序为:c、b、a
④反应2A(s)+B(g)=2C (g)+D(g)不能自发进行,则该反应△H一定大于0
⑤已知醋酸电离平衡常数为Ka:醋酸根水解常数为Kb;水的离子积为Kw:则三者关系为:KaKb=Kw
⑥反应A(g)=2B(g) △H,若正反应的活化能为EakJmol-1,逆反应的活化能为EbkJmol-1,则△H=(Ea-Eb)kJmol-1上述归纳正确的是( )
A.全部B.③④⑤⑥C.②④⑤⑥D.①②④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com