
| A£® | pH=0µÄČÜŅŗ£ŗFe2+”¢Br-”¢Na+”¢NO3- | |
| B£® | ÓÉĖ®µēĄė²śÉśµÄc£ØH+£©=1.0”Į10-12mol•L-1µÄČÜŅŗÖŠ£ŗK+”¢AlO2-”¢NO3-”¢Na+ | |
| C£® | ÖŠŠŌČÜŅŗÖŠ£ŗFe3+”¢K+”¢Al3+”¢SO42- | |
| D£® | ŌŚ0.1 mol•L-1Na2CO3ČÜŅŗÖŠ£ŗA1O2-”¢Na+”¢NO3-”¢C1- |
·ÖĪö A£®pH=0µÄČÜŅŗĪŖĖįŠŌČÜŅŗ£¬ĻõĖįøłĄė×ÓŌŚĖįŠŌĢõ¼žĻĀÄܹ»Ńõ»ÆŃĒĢśĄė×ÓŗĶäåĄė×Ó£»
B£®ÓÉĖ®µēĄė²śÉśµÄc£ØH+£©=1.0”Į10-12mol•L-1µÄČÜŅŗĪŖĖįŠŌ»ņ¼īŠŌČÜŅŗ£¬Ę«ĀĮĖįøłĄė×ÓÓėĖįŠŌČÜŅŗÖŠµÄĒāĄė×Ó·“Ó¦£»
C£®ĢśĄė×Ó”¢ĀĮĄė×ÓÖ»ÄÜ“ęŌŚÓŚÖŠŠŌČÜŅŗÖŠ£»
D£®ĖÄÖÖĄė×ÓÖ®¼ä²»·“Ó¦£¬¶¼²»ÓėĢ¼ĖįÄĘ·“Ó¦£®
½ā“š ½ā£ŗA£®pH=0µÄČÜŅŗĪŖĖįŠŌČÜŅŗ£¬NO3-ŌŚĖįŠŌĢõ¼žĻĀÄܹ»Ńõ»ÆFe2+”¢Br-£¬ŌŚČÜŅŗÖŠ²»ÄÜ“óĮæ¹²“ę£¬¹ŹA“ķĪó£»
B£®ÓÉĖ®µēĄė²śÉśµÄc£ØH+£©=1.0”Į10-12mol•L-1µÄČÜŅŗÖŠ“ęŌŚµēĄėĒāĄė×Ó»ņĒāŃõøłĄė×Ó£¬AlO2-ÓėĒāĄė×Ó·“Ó¦£¬ŌŚĖįŠŌČÜŅŗÖŠ²»ÄÜ“óĮæ¹²“ę£¬¹ŹB“ķĪó£»
C£®Fe3+”¢Al3+Ö»ÄÜ“ęŌŚÓŚĖįŠŌČÜŅŗ£¬ŌŚÖŠŠŌČÜŅŗÖŠ²»ÄÜ“óĮæ¹²“ę£¬¹ŹC“ķĪó£»
D£®A1O2-”¢Na+”¢NO3-”¢C1-Ö®¼ä²»·¢Éś·“Ó¦£¬¶¼²»ÓėNa2CO3·“Ó¦£¬ŌŚČÜŅŗÖŠÄܹ»“óĮæ¹²“ę£¬¹ŹDÕżČ·£»
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²éĄė×Ó¹²“ęµÄÅŠ¶Ļ£¬ĪŖøßæ¼µÄøßʵĢā£¬ŹōÓŚÖŠµČÄѶȵďŌĢā£¬×¢ŅāĆ÷Č·Ąė×Ó²»ÄÜ“óĮæ¹²“ęµÄŅ»°ćĒéæö£¬Čē£ŗÄÜ·¢Éśø“·Ö½ā·“Ó¦µÄĄė×ÓÖ®¼ä£»ÄÜ·¢ÉśŃõ»Æ»¹Ō·“Ó¦µÄĄė×ÓÖ®¼äµČ£»»¹Ó¦øĆ×¢ŅāĢāÄæĖłŅžŗ¬µÄĢõ¼ž£¬Čē£ŗČÜŅŗµÄĖį¼īŠŌ£¬¾Ż“ĖĄ“ÅŠ¶ĻČÜŅŗÖŠŹĒ·ńÓŠ“óĮæµÄ H+»ņOH-£»ČÜŅŗµÄ¾ßĢå·“Ó¦Ģõ¼ž£¬Čē”°Ńõ»Æ»¹Ō·“Ó¦”±”¢”°¼ÓČėĀĮ·Ū²śÉśĒāĘų”±£»ŹĒ”°æÉÄÜ”±¹²“ę£¬»¹ŹĒ”°Ņ»¶Ø”±¹²“ęµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µČÖŹĮæµÄĮ½ĪļÖŹ·Ö±šÓė×ćĮæŃĪĖį³ä·Ö·“Ó¦Ź±£¬NaHCO3²śÉśCO2ĘųĢå¶ą | |
| B£® | æÉŅŌÓĆ³ĪĒåŹÆ»ŅĖ®»ņÕßĒāŃõ»ÆÄĘČÜŅŗĒų±š | |
| C£® | µČÖŹĮæµÄĮ½ĪļÖŹ·Ö±šÓė×ćĮæµÄµČÅضČŃĪĖį·“Ó¦Ź±£¬Ņ»°ćŹĒNa2CO3²śÉśCO2ĘųĢåæģ | |
| D£® | NaHCO3ÖŠNa2CO3»ģÓŠŌÓÖŹæÉŅŌÓĆ¼ÓČČ·½·Ø³żČ„ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 ÄÜŌ“ŹĒµ±½ńÉē»į·¢Õ¹µÄČż“óÖ§ÖłÖ®Ņ»£¬ÓŠ×ؼŅÖø³ö£ŗČē¹ū¶ŌČ¼ĮĻ²śĪļČēCO2”¢H2O”¢N2µČÄܹ»ŹµĻÖĄūÓĆĢ«ŃōÄÜČĆĖüĆĒÖŲŠĀ×éŗĻ£ØČēĶ¼£©£¬æÉŅŌ½ŚŌ¼Č¼ĮĻ£¬»ŗ½āÄÜŌ“Ī£»ś£®ŌŚ“Ė¹¹ĻėµÄĪļÖŹŃ»·ÖŠĢ«ŃōÄÜ×īÖÕ×Ŗ»Æ£Ø””””£©
ÄÜŌ“ŹĒµ±½ńÉē»į·¢Õ¹µÄČż“óÖ§ÖłÖ®Ņ»£¬ÓŠ×ؼŅÖø³ö£ŗČē¹ū¶ŌČ¼ĮĻ²śĪļČēCO2”¢H2O”¢N2µČÄܹ»ŹµĻÖĄūÓĆĢ«ŃōÄÜČĆĖüĆĒÖŲŠĀ×éŗĻ£ØČēĶ¼£©£¬æÉŅŌ½ŚŌ¼Č¼ĮĻ£¬»ŗ½āÄÜŌ“Ī£»ś£®ŌŚ“Ė¹¹ĻėµÄĪļÖŹŃ»·ÖŠĢ«ŃōÄÜ×īÖÕ×Ŗ»Æ£Ø””””£©| A£® | »ÆѧÄÜ | B£® | ČČÄÜ | C£® | ÉśĪļÄÜ | D£® | µēÄÜ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
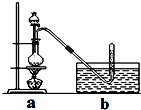
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
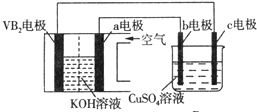
| A£® | µē½ā¹ż³ĢÖŠ£¬cµē¼«±ķĆęĻČÓŠŗģÉ«ĪļÖŹĪö³ö£¬ŗóÓŠĘųÅŻ²śÉś | |
| B£® | ĶāµēĀ·ÖŠµē×ÓÓÉcµē¼«Į÷ĻņVB2µē¼« | |
| C£® | VB2µē¼«·¢ÉśµÄµē¼«·“Ó¦ĪŖ£ŗ2VB2+11H2O-22e-ØTV2O5+2B2O3+22H+ | |
| D£® | ČōB×°ÖĆÄŚµÄŅŗĢåĢå»żĪŖ100 mL£¬ŌņCuSO4ČÜŅŗµÄĪļÖŹµÄĮæÅضČĪŖ0.05 mol/L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
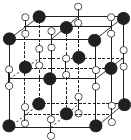 I£®µŖ×åŌŖĖŲŗĶĀ±×åŌŖĖŲ¶¼ÄÜŠĪ³ÉŠķ¶ąÖÖĪļÖŹ£®
I£®µŖ×åŌŖĖŲŗĶĀ±×åŌŖĖŲ¶¼ÄÜŠĪ³ÉŠķ¶ąÖÖĪļÖŹ£®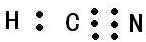 £»ĘäÖŠŠÄCŌ×ÓµÄŌÓ»ÆĄąŠĶĪŖsp£®µŖ”¢Į×”¢·śČżÖÖŌŖĖŲµÄµēøŗŠŌÓɓ󵽊”µÄĖ³ŠņĪŖF£¾N£¾P£ØÓĆŌŖĖŲ·ūŗűķŹ¾£©£®
£»ĘäÖŠŠÄCŌ×ÓµÄŌÓ»ÆĄąŠĶĪŖsp£®µŖ”¢Į×”¢·śČżÖÖŌŖĖŲµÄµēøŗŠŌÓɓ󵽊”µÄĖ³ŠņĪŖF£¾N£¾P£ØÓĆŌŖĖŲ·ūŗűķŹ¾£©£®| F | Cl | Br | I | |
| µŚŅ»µēĮ¦ÄÜ£ØkJ•mol-1£© | 1681 | 1251 | 1140 | 1008 |
| ¾§Ģå | NaCl | KCl | CaO |
| ¾§øńÄÜ£ØkJ•mol-1£© | 786 | 715 | 3401 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com