
【题目】某同学配置450毫升 1mol/L的硫酸溶液
(1)应该选择________的容量瓶 A 250毫升 B 500毫升 C 1000毫升
(2)需要量取98%,ρ=1.84g/cm3浓硫酸__________毫升
(3)将所取浓硫酸逐滴加入盛有水的烧杯中,边加边搅拌
(4)将该溶液注入容量瓶
(5)在容量瓶中加水至___________处,改用__________加水至_______与刻度线相切
(6)塞好瓶塞,反复摇匀
(7)摇匀后发现,溶液体积缩小,继续加水至刻度线
(8)该同学的操作是否有不当之处,请指出(不必全部填满)
a__________________该错误操作将使所配溶液的浓度_______(“变大”或“变小”)
b____________该错误操作将使所配溶液的浓度_______(“变大”或“变小”)
c_______________该错误操作将使所配溶液的浓度_______(“变大”或“变小”)
d____________该错误操作将使所配溶液的浓度_______(“变大”或“变小”)
【答案】B 27.2 离刻度线1-2cm 胶头滴管 凹液面的最低处 未冷却至室温 变大 未用玻璃棒引流 变小 未洗涤烧杯并将洗涤液转移入容量瓶 变小 摇匀后再加水 变小
【解析】
(1)根据常见容量瓶的规格选择容量瓶;
(2)根据c=![]() 计算浓硫酸的物质的量浓度,再根据溶液稀释前后物质的量不变计算所需浓硫酸的体积;
计算浓硫酸的物质的量浓度,再根据溶液稀释前后物质的量不变计算所需浓硫酸的体积;
(5)定容时先直接加水,再改用胶头滴管加水;
(8)结合具体操作和c=![]() 分析引起的误差。
分析引起的误差。
(1)因无450mL的容量瓶,则配置450毫升 1mol/l的硫酸溶液应选择500mL容量瓶,故答案为B;
(2)98%浓硫酸的密度为1.84gcm-3,其物质的量浓度=![]() =18.4mol/L,设需要浓硫酸体积为V,则根据溶液稀释前后物质的量不变,V×18.4mol/L=1.0molL-1×500mL,解得V=27.2mL;
=18.4mol/L,设需要浓硫酸体积为V,则根据溶液稀释前后物质的量不变,V×18.4mol/L=1.0molL-1×500mL,解得V=27.2mL;
(5)定容时,在容量瓶中加水至离刻度线1-2cm处,改用胶头滴管加水至凹液面的最低处与刻度线相切即可;
(8)a.浓硫酸稀释后未冷却即可转移到容量瓶,则定容后溶液温度降低,液面下降,溶液体积偏小,导致所配溶液的浓度变大;
b.向容量瓶内转移溶液时未用玻璃棒引流,会有少量溶液溅到容量瓶外,溶质的量减小,导致所配溶液的浓度变小;
c.转移硫酸溶液后,未洗涤烧杯并将洗涤液转移入容量瓶,溶质的量减小,导致所配溶液的浓度变小;
d.摇匀后再加水,将使溶液的体积偏大,导致所配溶液的浓度变小。


科目:高中化学 来源: 题型:
【题目】依据图中氮元素及其化合物的转化关系,回答问题:
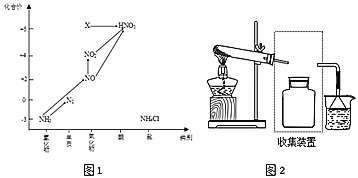
(1)图1中,X的化学式为_____,从化合价上看,X具有______性(“氧化”、“还原”)。
(2)回答下列关于NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为__________。
②下列试剂不能用于干燥NH3的是__________(填字母)。
A.浓硫酸 B.碱石灰 C.生石灰
③若要收集一瓶氨气,采用的方法是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素 W、X、Y、Z 的原子序数依次增大,W、X 原子的最外层电子数之比为 4:3,Z 原子比 X 原子的核外电子数多 4。下列说法正确的是
A.W、Y、Z 的电负性大小顺序一定是 Z>Y>W
B.W、X、Y、Z 的原子半径大小顺序可能是 W>X>Y>Z
C.Y、Z 形成的分子空间构型可能是正四面体
D.WY2 分子中![]() 键与π键的数目之比是 2:1
键与π键的数目之比是 2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过对煤的综合利用,可以获得多种有机物。化合物A含有碳、氢、氧3种元素,其质量比是12:3:8。液态烃B是一种重要的化工原料,其摩尔质量为78 gmol-1。E是有芳香气味的酯。它们之间的转化关系如下(含有相同官能团的有机物通常具有相似的化学性质):
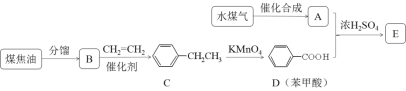
请回答:
(1)化合物A所含的官能团名称是_____________。
(2)B和CH2=CH2反应生成C的反应类型是_____________。
(3)E在氢氧化钠溶液中水解的化学方程式是_____________。
(4)下列说法正确的是_____________。
A.将铜丝在空气中灼烧后迅速插入A中,反应多次,可得到能发生银镜反应的物质
B.在一定条件下,C可通过取代反应转化为![]()
C.苯甲酸钠(常用作防腐剂)可通过D和氢氧化钠反应得到
D.共a mol的B 和D混合物在氧气中完全燃烧,消耗氧气大于7.5a mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸乙酯是无色透明有香味的液体,制备的实验装置如图所示。下列说法不正确的是( )
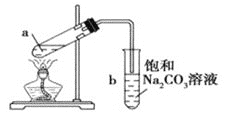
A.先在试管a中加入乙醇,然后边振荡试管边缓慢加入浓硫酸,待冷却后加入乙酸
B.浓硫酸的作用主要是催化剂和吸水剂
C.b中的饱和Na2CO3溶液可用浓NaOH溶液代替
D.试管b中导气管下端管口不能浸入液面的原因是防止实验过程中发生倒吸现象
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,改变0.1mol·L-1的富马酸(H2A)溶液的pH,溶液中的H2A、HA-、A2-的物质的量分数δ(X)[ δ(X)= ![]() ]随pH的变化如图所示。下列叙述正确的是( )
]随pH的变化如图所示。下列叙述正确的是( )
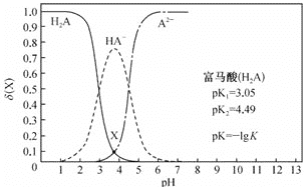
A.pH=3.05时,c(H2A)=c(HA-)=c(OH-)B.pH=4.0时, c(HA-)>C(H2A)>c(A2-)
C.常温下,反应HA-+OH-![]() A2-+H2O的pK=9.51D.常温下,图中x点处:1g
A2-+H2O的pK=9.51D.常温下,图中x点处:1g![]() =0.72
=0.72
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设A、B、C代表三种元素,已知①B2―和A+两种离子具有相同的电子层结构,②C元素的原子核内质子数比B元素的原子核内质子数少8个,③B和C两种元素可形成5个原子核(一般简称5核)50个电子的负二价阴离子(提示为:BC42―或为:CB42―)。据此填空:
(1)写出B和C的元素名称:B为_____________,C为_____________。
(2)有A、B、C三种元素形成的含78个电子的盐类化合物的化学式是______________。
(3)某元素X的原子与A元素形成的化合物的化学式为:AX,通过测量发现的式量为76,X原子核内中子数为20,则X属于的元素名称是_____________,用化学符号表示X原子应该是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于常温下pH= 3的乙酸溶液,下列说法正确的是
A.c(H+)=c(CH3COO-)+c(OH-)
B.加水稀释到原体积的10倍后溶液pH变为4
C.加入少量乙酸钠固体,溶液pH降低
D.与等体积pH=11的NaOH溶液混合后所得溶液中c(Na+)=c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温条件下,下列各组离子在相应的条件下可能大量共存的是( )
A.能使pH试纸变红的溶液中:CO32-、K+、Cl-、Na+
B.由水电离产生的c(OH-)=1×10-10 mol·L-1的溶液中:NO3-、Mg2+、Na+、SO42-
C.在c(OH-)/c(H+)=1×1012的溶液中:NH4+、Fe3+、Cl-、NO3-
D.![]() =10-10 mol·L-1的溶液中:Na+、HCO3-、Cl-、K+
=10-10 mol·L-1的溶液中:Na+、HCO3-、Cl-、K+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com