
【题目】金属钛(Ti)被誉为21世纪金属,其单质和化合物具有广泛的应用价值。
请回答下列问题:
(1)Ti的基态原子价电子排布式为______。
(2)纳米TiO2常用作下述反应的催化剂。

化合物甲的分子中采取sp2方式杂化的碳原子有_____________个,化合物乙中采取sp3方式杂化的原子对应的元素的电负性由大到小的顺序为___________________。
(3)含Ti3+的配合物的化学式为[TiCl(H2O)5]Cl2·H2O,其配离子中含有的化学键类型是____________,1 mol该配合物中含有的![]() 键数目是____________。
键数目是____________。
(4)通过X—射线探知KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似。且知三种 离子晶体的晶格能数据如下:

KCl、MgO、CaO、TiN四种离子晶体熔点由高到低的顺序为______________________。
(5)某种氮化钛晶体的晶胞如图所示,该晶体中与N原子距离相等且最近的N原子有_____个:Ti原子的配位数为______;此配位原子构成的空间构型为_____;该晶胞中N、Ti原子之间的最近距离为a nm。则该氮化钛晶体的密度为______g·cm-3、NA为阿伏加德罗常数的值,只列计算式)。

【答案】 3d24s2 7 O>N>C 配位键、极性共价键 18NA TiN>MgO>CaO>KCl 12 6 正八面体 ![]() 。
。
【解析】(1)本题考查价电子和电子排布式,Ti属于过渡元素,价电子包括最外层电子和次外层d能级上的电子,即价电子排布式为3d24s2;(2)本题考查杂化类型和电负性的规律,苯环上的碳原子为sp2杂化,连有羟基的碳原子和甲基上的碳原子有4个σ键,无孤电子对,其杂化类型是sp3杂化,羰基上的碳原子有3个σ键,无孤电子对,其杂化类型为sp2杂化,因此有机物甲有7个sp2杂化的碳原子,化合物乙中采用sp3杂化的是,羟基连接的碳原子、甲基上的碳原子、N、O,同周期从左向右电负性增强,即O>N>C;(3)本题考查化学键的类型,Cl-和H2O与Ti3+形成配位键,H2O中H和O之间形成(极性)共价键;配离子中Cl-与Ti3+形成1molσ键,配离子中有5mol水分子,1mol水分子有2molσ键,水分子共形成10molσ键,5mol水与Ti3+形成5molσ键,此配合物中还含有结晶水,因此1mol配合物中含有σ键的数目是18NA;(4)考查晶格能,离子晶体熔沸点与晶格能有关,晶格能与离子半径和所带电荷数有关,离子半径越小,所带电荷数越多,晶格能越大,晶体的熔沸点越高,TiN所带电荷数最多,晶格能最大,MgO和CaO中Mg2+的半径小于Ca2+,MgO的熔点大于CaO,NaCl所带电荷数最少,因此熔点由高到低的顺序是TiN>MgO>CaO>KCl;(5)考查晶胞的结构和计算,根据晶胞的结构,与N距离相等且最近的N原子有12个,上层4个,中间4个,下层4个;离子晶体的配位数为一个离子周围最近的异性离子的个数,即Ti的配位数为6;构成的空间构型为正八面体;N位于晶胞的顶点、面心,个数为8×1/8+6×1/2=4个,Ti位于棱上和体心,个数为12×1/4+1=4,化学式为TiN,晶胞的质量为4×62/NAg,晶胞的边长是N、Ti原子之间的最近距离的2倍,则晶胞的体积为(2a×10-7)cm3,则晶胞的密度为![]() g/cm3。
g/cm3。


 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:
【题目】氧化锌、硫化锌都是重要的基础化工原料。
(1)ZnO 与 Al2O3 的化学性质相似,ZnO 在 NaOH 溶液中转化成[Zn(OH)4]2的离子方程式为_____________。
(2)火法炼锌得到的氧化锌中含有铅、铜等杂质,提纯步骤如下:
![]()
![]()
①上图中的“冷凝物”为________(填化学式)。
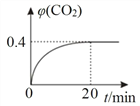
②某温度时,在反应Ⅰ的反应炉中,起始时 c(CO)为 0.3 molL1,反应过程中 CO2 的体积分数 φ(CO2)如图所示,则反应Ⅰ的平衡常数 K=_____。
③下列措施有利于提高反应Ⅰ中 ZnO 转化率的是________。
a.增大 ZnO 的投料量 b.适当加压 c.将锌蒸气及时分离
④反应Ⅱ中,每转移 1mol 电子,反应放热 174 kJ,则 H2=_____________。
(3)测定氧化锌样品纯度:称取 0.5000g 样品,酸溶后定容于 250 mL 容量瓶中,摇匀。量取 25.00 mL 该溶液,用 0.04000 molL1 的 EDTA(Na2H2Y)标准液滴定其中的 Zn2+(反应方程式为 Zn2++H2Y2=ZnY2+2H+,杂质不反应),平行滴定三次,平均消耗 EDTA 标准液 15.12mL。
①若滴定管未用 EDTA 标准液润洗,测定结果将___(填“偏高”、“偏低”或“不变”)。
②样品纯度为:________________(列出计算式即可)。
(4)彩电荧光屏中的蓝色荧光粉含有 ZnS。将含有 0.05mol ZnS 的荧光粉溶于 500mL盐酸中,完全溶解后,溶液中 c(S2)≤__________ molL1。(已知:Ksp(ZnS)=2.5×1023,忽略溶液体积的变化)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学在人类生活中扮演着重要角色,下列应用不正确的是( )
A.明矾可用于水的杀菌,消毒
B.盐卤可用于制豆腐
C.目前加碘食盐主要添加的是KIO3
D.在空气质量日报中SO2含量属于空气污染指数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于CH4和CO2的说法正确的是
A. 固态CO2属于原子晶体
B. CH4分子中含有极性共价键,是极性分子
C. 因为碳氢键键能小于碳氧键,所以CH4熔点低于CO2
D. CH4和CO2分子中碳原子的杂化类型分别是sp3和sp
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组为研究电化学原理,设计如图装置.下列叙述不正确的是( )
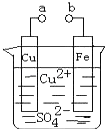
A.a和b不连接时,铁片上会有金属铜析出
B.a和b用导线连接时,铜片上发生的反应为:Cu2++2e﹣=Cu
C.无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成 浅绿色
D.a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学电池的说法中正确的是
A.化学电池只能将化学能转化为电能
B.燃料电池能将全部化学能转化为电能
C.锌银电池比能量大,电压稳定,储存时间长
D.一次电池包括干电池和蓄电池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物H为芳香酯,其合成路线如下:
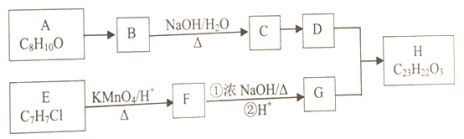
已知以下信息:
①A—H均为芳香族化合物,A的苯环上只有一个取代基,B能发生银镜反应,D的相对分子质量比C大4,E的核磁共振氢谱有3组峰。
② 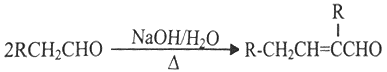
③
请回答下列问题:
(1)A→B的反应类型为____________,G所含官能团的名称为 ________________。
(2)B与银氨溶液反应的化学方程式为_____________________。
(3)H的结构简式为____________。
(4)符合下列要求的A的同分异构体有________________种。
①遇氯化铁溶液显紫色 ②属于芳香族化合物
其中苯环上有两个取代基的有 ___________________ (写结构简式)
(5)根据已有知识并结合相关信息,写出以CH3CH2OH为原料制备CH3CH2CH2CH2OH的合成路线流程图(无机试剂任用)______________合成路线流程图示例如下:
CH3CH2Br ![]() CH3CH2OH
CH3CH2OH ![]() CH3COOCH2CH3
CH3COOCH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某物质只含C、H、O三种元素,其分子模型如图所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键)。

(1)该物质的结构简式为___________________。
(2)该物质中所含官能团的名称为_____________________。
(3)下列物质中,与该产品互为同系物的是__________________,与该产品互为同分异构体的是__________________。(填序号)
①CH3CH="==CHCOOH"
②CH2===CHCOOCH3
③CH3CH2CH===CHCOOH
④CH3CH(CH3)COOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com