
【题目】已知烯烃在一定条件下可被强氧化剂氧化,例如:
(1)RCH=CHR′![]() RCHO + R′CHO,
RCHO + R′CHO,
![]()
从A出发有下图所示关系:
![]()
已知,A不含-CH3。E的分子式为C9H10O2。
(1)A的分子式为____________________,E的结构简式为__________________________。A→C的化学反应方程式为________________________________________________。
(2)若B的一种同分异构体跟溴水反应生成白色沉淀,且1mol该同分异构体跟溴水反应时,需消耗3mol Br2,则符合该条件的同分异构体有__________种,写出其中任意一种的结构简式:____________________________;
(3)A是一种可以作为药物的有机物,将A在一定条件下氧化可以得到两种有机酸X和Y,X属于芳香族化合物,它在食品保存及染料、药物生产中均有重要作用,则X与Y的结构简式分别为:_______________,____________________。
(4)由A制E还可以通过以下途径:

①设计步骤A→F的目的是___________;
②写出G→H的化学反应方程式:_______________________________________________。
【答案】 C9H8O ![]()
![]() + 2Ag(NH3)2OH
+ 2Ag(NH3)2OH![]()
![]() + 2Ag↓+3NH3 + H2O 3
+ 2Ag↓+3NH3 + H2O 3 ![]() 或
或 ![]() 或
或 ![]()
![]() HOOC-COOH 保护碳碳双键,防止下一步被氧化造成碳链断开
HOOC-COOH 保护碳碳双键,防止下一步被氧化造成碳链断开 ![]() + 2NaOH
+ 2NaOH![]()
![]() + NaBr + 2H2O或
+ NaBr + 2H2O或 ![]() + 2NaOH
+ 2NaOH ![]()
![]() + NaBr + 2H2O
+ NaBr + 2H2O
【解析】A与E中C原子数相等,所以A中含有9个C原子,因不含-CH3,且能发生银镜反应,所以A中存在-CHO,A还能与2molH2发生加成反应,说明A中含有1个碳碳双键,由E的分子式可推知A为![]() ,其分子式为C9H8O,B为
,其分子式为C9H8O,B为![]() ,C为
,C为![]() ,D为
,D为![]() ,E为
,E为![]() ,
,![]() 与HBr发生加成反应生成
与HBr发生加成反应生成![]() 或
或![]() ,由于氧化醛基的同时碳碳双键也能被氧化,则A→F的目的是保护碳碳双键,则G为
,由于氧化醛基的同时碳碳双键也能被氧化,则A→F的目的是保护碳碳双键,则G为![]() 或
或![]() ,在NaOH的醇溶液中发生消去反应生成H为
,在NaOH的醇溶液中发生消去反应生成H为![]() ,酸化后I为
,酸化后I为![]() ,则
,则
(1)由以上分析可知A的化学式为C9H8O,E的结构简式为![]() ,A→C的化学反应方程式为
,A→C的化学反应方程式为 ;(2)B的一种同分异构体跟溴水反应生成白色沉淀,且1mol该同分异构体跟溴水反应时,需要消耗3molBr2,说明酚羟基的邻位、对位不存在取代基,则可能的同分异构体有3种,分别为
;(2)B的一种同分异构体跟溴水反应生成白色沉淀,且1mol该同分异构体跟溴水反应时,需要消耗3molBr2,说明酚羟基的邻位、对位不存在取代基,则可能的同分异构体有3种,分别为![]() 或
或 ![]() 或
或 ![]() (任写一种);(3)根据题目信息,
(任写一种);(3)根据题目信息,![]() 在催化氧化下生成两种物质:
在催化氧化下生成两种物质:![]() 和HOOC-COOH,则X的结构简式为
和HOOC-COOH,则X的结构简式为![]() ,Y的结构简式为HOOC-COOH;(4)①由于氧化醛基的同时碳碳双键也能被氧化,则A→F的目的是保护碳碳双键,防止下一步被氧化,从而造成碳链断开;②G为
,Y的结构简式为HOOC-COOH;(4)①由于氧化醛基的同时碳碳双键也能被氧化,则A→F的目的是保护碳碳双键,防止下一步被氧化,从而造成碳链断开;②G为![]() 或
或![]() ,在NaOH的醇溶液中发生消去反应生成H,反应的方程式为
,在NaOH的醇溶液中发生消去反应生成H,反应的方程式为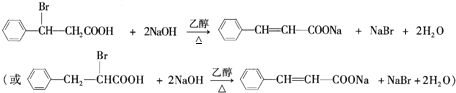 。
。


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 1molO2在任何情况下都是32g B. 摩尔是一个基本物理量
C. H2SO4的摩尔质量是98g D. 1摩尔氢的质量是2g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、前20号元素A、B、C、D,其中A元素所处的周期数、主族序数、原子序数均相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C。
(1)C在周期表中的位置__________________________;
(2)B 元素的原子结构示意图____________________________;
(3)化合物D2C的电子式______________________________;
(4)B最简单气态氢化物与最简单的有机物的稳定性强弱关系(用相应的化学式表示):____ > ____;
(5)C、D离子的半径大小关系为C______D (填:>、=、<);
(6)B的氢化物与B的最高价氧化物对应水化物反应的生成物中含有的的化学键有__________填选项)。
A、只含离子键 B、既有离子键又有共价健
C、只含有共价键 D、既有极性共价键又有非极性共价键
Ⅱ、利用下图装置来验证同主族元素非金属性的变化规律:

(1)要证明非金属性:Cl>I,在A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾溶液,观察到C中溶液现象是:___________,即可证明。干燥管D的作用是___________________。从环境保护的角度考虑,此装置尚缺少尾气处理装置,可用_________________溶液吸收尾气。
(2)要证明非金属性:C>Si,在A中加盐酸,B中加CaCO3,C中加Na2SiO3溶液,将观察到C中______________的现象。但老师认为,该现象不足以证明酸性强弱关系为碳酸>硅酸,因此应在B、D之间增加一个盛有足量__________的洗气装置(选填下列字母)
A.浓盐酸 B.浓NaOH溶液 C.饱和Na2CO3溶液 D.饱和NaHCO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 可简写为
可简写为 。现有某化合物W的分子结构可表示为
。现有某化合物W的分子结构可表示为![]() 。
。
(1)W的一氯代物有_________种。
(2)下列有关W的说法不正确的是____________(填编号);
a.能发生还原反应
b.能发生氧化反应
c.能发生加聚反应
d.等质量的W与苯分别完全燃烧所消耗的氧气量,前者大
(3)写出W的芳香族同分异构体(能发生聚合反应)的结构简式____________,该聚合反应的化学方程式为______________________________________________。
(4)W属于____________(填编号)。
a.芳香烃 b.环烃 c.不饱和烃 d.炔烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据元素周期表判断下列描述正确的是
A. 第VIII族是包含元素种类最多的族
B. 第VIA族元素形成的化合物种类最多
C. 每个短周期都既包含金属元素也包含非金属元素
D. 在金属和非金属元素分界线附近可以寻找制作半导体材料的元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应有多种分类方法,其中根据参与电子转移的元素种类不同的分类方法最常见。下列反应中电子转移发生在相同价态的同种元素之间的有________;电子转移发生在不同价态的同种元素之间的有________;电子转移发生在不同元素之间的有________。(填反应编号)
(1)Fe+2FeCl3![]() 3FeCl2
3FeCl2
(2)NH4NO3![]() N2O↑+2H2O
N2O↑+2H2O
(3)2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
(4)S+2KNO3+3C![]() K2S+N2↑+3CO2↑
K2S+N2↑+3CO2↑
(5)Cl2+2NaOH![]() NaCl+NaClO+H2O
NaCl+NaClO+H2O
(6)HgS+O2![]() Hg+SO2
Hg+SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中含有的化学键类型完全相同的是
A. MgCl2、KOH B. AlCl3、HCl
C. H2O2、CS2 D. CaO2、CaCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某一反应体系中有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2。
(1)该反应中的还原剂是 。
(2)该反应中,发生还原反应的过程是 → 。
(3)写出该反应的化学方程式,并用双线桥法标出电子转移的方向和数目: 。
(4)若反应转移了0.3 mol电子,则产生的气体在标准状况下体积为 L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com