
分析 等体积的0.15mol/L的BaCl2溶液,可使相同体积的Fe2(SO4)3、Na2SO4、KAl(SO4)2三种溶液的SO42-完全沉淀,则Fe2(SO4)3、Na2SO4、KAl(SO4)2三种溶液中n(SO42-)相同,根据硫酸根守恒可知,n[Fe2(SO4)3]=$\frac{1}{3}$n(SO42-),n(Na2SO4)=n(SO42-),n[KAl(SO4)2]=$\frac{1}{2}$n(SO42-),三种溶液的体积相同,物质的量浓度之比等于溶质物质的量之比,以此解答该题.
解答 解:等体积的0.1mol/L的BaCl2溶液,可使相同体积的Fe2(SO4)3、Na2SO4、KAl(SO4)2三种溶液的SO42-完全沉淀,则Fe2(SO4)3、Na2SO4、KAl(SO4)2三种溶液中n(SO42-)相同,根据硫酸根守恒可知,n[Fe2(SO4)3]=$\frac{1}{3}$n(SO42-),n(Na2SO4)=n(SO42-),n[KAl(SO4)2]=$\frac{1}{2}$n(SO42-),三种溶液的体积相同,物质的量浓度之比等于溶质物质的量之比,所以三种硫酸盐的物质的量浓度之比为c(Na2SO4):c[Fe2(SO4)3]:c[KAl(SO4)2]=n(SO42-):$\frac{1}{3}$n(SO42-):$\frac{1}{2}$n(SO42-)=6:2:3,
故答案为:6:2:3.
点评 本题考查物质的量浓度的计算、反应方程式的计算等,为高频考点,侧重考查学生的分析、计算能力,难度不大,根据化学式推断溶质的物质的量与硫酸根关系是解题关键.


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2和CO的混合气 | B. | C2H2O2 | C. | C3H6O3 | D. | C6H12O5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
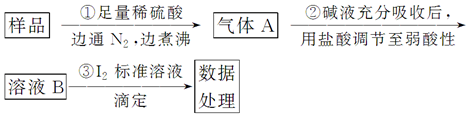
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
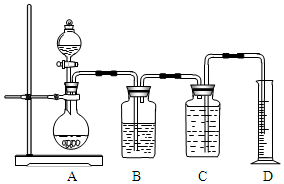 如图所示装置可用于多种实验.
如图所示装置可用于多种实验.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
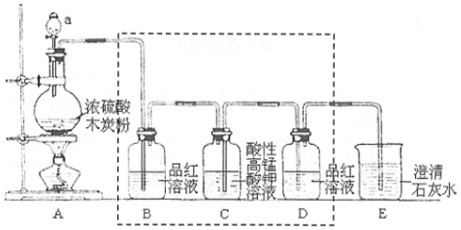
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeSO4溶液存放在加有少量铁粉的试剂瓶中 | |
| B. | 将1mol/L的NaCl溶液保存在容量瓶中 | |
| C. | 凡是给玻璃仪器加热,都要垫石棉网,以防仪器炸裂 | |
| D. | 用pH试纸检验某溶液的酸碱性时,一定要先用蒸馏水湿润 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com