���
�⣺M�������ֺ��ݣ�N�������ֺ�ѹ�����ڷ�Ӧǰ�������ϵ���Ͳ��ȣ���������ƽ��̬Ҳ��һ����
A��Ҫ��M��N��ƽ��ʱA���������һ������ôֻ����M��N�У���Ӧǰ�����ȶ��٣�A���������ʼ��Ϊ��ֵ���ٶ���Ӧ��AΪzmol����
A��g��+3B��g��?2C��g��
��ʼ��x y
��Ӧ��z 3z 2z
ƽ�⣺x-z y-3z 2z
��ƽ��ʱA���������Ϊ
��A���������ʼ��Ϊ��ֵ����x=y����A��ȷ��
B��x��y=1��2����y=2 x���跴Ӧ�����ĵ�amolA����
A��g��+3B��g��?2C��g��
��ʼ��mol����x 2x 0
�仯��mol����a 3a 2a
��A��ת����=
��B��ת����=
����ƽ��ʱ��M�е�ת���ʣ�A��B����B����
C����Ŀ���Ȼ�ѧ����ʽ�����壺��1molA��ȫ��Ӧ������192 kJ����M�зų�����172.8 kJʱ���μӷ�Ӧ��A�����ʵ���Ϊ
��1mol=0.9mol����A��ת����Ϊ
����C����
D��x=1.2��y=1��N�дﵽƽ��ʱ���Ϊ2 L������C 0.4 mol����
A��g��+3B��g��?2C��g��
��ʼ��1.2 1
��Ӧ��0.2 0.6 0.4
ƽ�⣺1 0.4 0.4
��A��B��C��ƽ��Ũ�ȷֱ�Ϊ0.5mol/L��0.2mol/L��0.2mol/L��
��ƽ�ⳣ��K=
=10
ԭƽ����ϵ�У�2.0L�����к��з������ʵ���Ϊ��1.0+0.4+0��mol=1.8mol��������0.36molA����ϵ˲���з������ʵ���Ϊ��1.8+0.36��mol=2.16mol��N�������¡���ѹ�������������=��������ʵ����ȣ�����2.16mol��1.8mol=V��2L��˲���������V����Ϊ
=2.4L����ʱ��Ũ����Qc=
=10.6��Qc��K�����ԣ�ƽ��Ҫ�����ƶ�����v��������v���棩����D��ȷ��
��ѡAD��

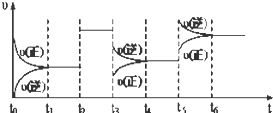
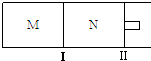 ��ͼ��ʾ������I�̶�������������������ƶ���M��N���������о�������Ӧ��A��g��+3B��g��?2C��g����H=-192kJ?mol-1����M��N�ж�ͨ��xmolA��ymolB�Ļ�����壬��ʼM��N�ݻ���ͬ�������¶Ȳ��䣮����˵����ȷ���ǣ�������
��ͼ��ʾ������I�̶�������������������ƶ���M��N���������о�������Ӧ��A��g��+3B��g��?2C��g����H=-192kJ?mol-1����M��N�ж�ͨ��xmolA��ymolB�Ļ�����壬��ʼM��N�ݻ���ͬ�������¶Ȳ��䣮����˵����ȷ���ǣ�������

 ���ѵ����Ԫ��ĩ���100��ϵ�д�
���ѵ����Ԫ��ĩ���100��ϵ�д� ��˼άС�ھ�100����ҵ��ϵ�д�
��˼άС�ھ�100����ҵ��ϵ�д� ��ʦָ��һ��ͨϵ�д�
��ʦָ��һ��ͨϵ�д�