
| A. | a=3.36时,CO2+2OH-→CO32-+H2O | |
| B. | a=4.48时,2CO2+3OH-→CO32-+HCO3-+H2O | |
| C. | a=5.60时,3CO2+4OH-→CO32-+2HCO3-+H2O | |
| D. | a=6.72时,CO2+OH-→HCO3- |
分析 少量二氧化碳,发生CO2+2OH-=CO32-+H2O,足量二氧化碳,发生CO2+OH-=HCO3-,结合反应的物质的量关系判断.
解答 解:n(NaOH)=0.1L×3mol/L=0.3mol,
A.a=3.36时,n(CO2)=0.15mol,发生CO2+2OH-=CO32-+H2O,故A正确;
B.a=4.48时,n(CO2)=0.2mol,由C原子守恒及电荷守恒可知,发生2CO2+3OH-=CO32-+HCO3-+H2O,故B正确;
C.a=5.60时,n(CO2)=0.25mol,3CO2+4OH-→CO32-+2HCO3-+H2O中,不符合物质的量关系,故C错误;
D.a=6.72时,n(CO2)=0.3mol,发生CO2+OH-=HCO3-,故D正确;
故选C.
点评 本题考查离子反应方程式的书写,为高频考点,把握发生的反应、离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意与量有关的判断,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
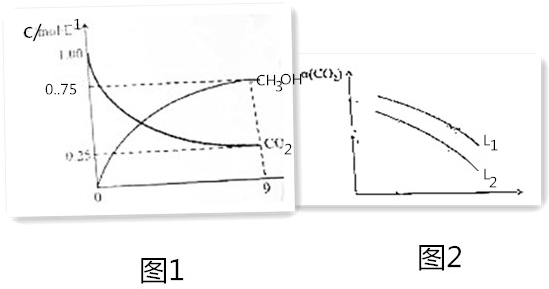
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
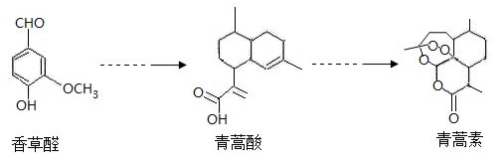
| A. | 青蒿素能发生水解反应 | |
| B. | 青蒿素易溶于乙醚 | |
| C. | 在一定条件下,香草醛可与HCHO发生缩聚反应 | |
| D. | 可用FeCl3 溶液或 NaHCO3溶液鉴别香草醛和青蒿酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 称量样品→加热→用已知质量的无水氯化钙吸收水蒸气并称量 | |
| B. | 称量样品→加热→冷却→称量Mg(NO3)2 | |
| C. | 称量样品→加热→冷却→称量MgO | |
| D. | 称量样品→加NaOH溶液→过滤→加热→冷却→称量MgO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中c(H+)=1.0×10-2 mol/L | |
| B. | 此溶液中由水电离出的c(OH-)=1.0×10-12 mol/L | |
| C. | 加水稀释100倍后,溶液的pH=4 | |
| D. | 加入等体积pH=12的氨水,溶液呈酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
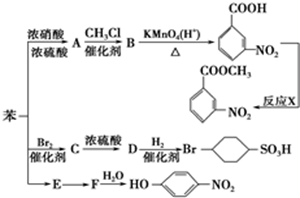
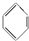 +HNO3(浓)$→_{△}^{浓硫酸}$
+HNO3(浓)$→_{△}^{浓硫酸}$ +H2O,其反应类型为取代反应.
+H2O,其反应类型为取代反应.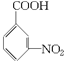 +CH3OH
+CH3OH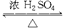
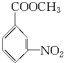 +H2O.
+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氮肥NH4NO3在重力撞击下可能发生爆炸 | |
| B. | 在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 | |
| C. | 单质硅可用于制备太阳能电池板,二氧化硅可用于制作光导纤维 | |
| D. | 聚酯纤维、碳纤维、光导纤维都属于有机高分子材料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com