
【题目】铝是地壳中含量最多的金属元素,它性能稳定,供应充足,铝—空气电池具有能量密度高、工作原理简单、成本低、无污染等优点。铝—空气电池工作原理示意图如图:
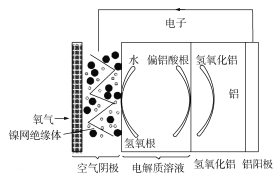
下列说法错误的是
A. 若是碱性电解质溶液中,则电池反应的离子方程式为:4Al+3O2+6H2O+4OH=4Al(OH)4-
B. 若是中性电解质溶液中,则电池反应的方程式为:4Al+3O2+6H2O=4Al(OH)3
C. 如果铝电极纯度不高,在碱性电解质溶液中会产生氢气
D. 若用该电池电解氯化钠溶液(石墨作电极),当负极减少5.4g时,阳极产生6.72L气体
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组在实验室中进行化学实验按右图甲,连接好线路发现灯泡不亮,按右图乙连接好线路发现灯泡亮,下列结论一定正确的是( )
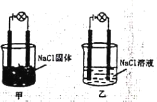
A.NaCl固体是非电解质而NaCl溶液是电解质
B.在通电的条件下,NaCl在水中电离出大量的离子而导电
C.相同条件下,向乙的NaCl溶液中逐滴滴加硝酸银溶液,溶液导电性先减弱后增强
D.甲的NaCl固体中无自由移动的阴阳离子,因此不能导电
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴及其化合物广泛应用于磁性材料、电池材料及超硬材料等领域。
(1)CoxNi(1-x)Fe2O4(其中Co、Ni均为+2)可用作H2O2分解的催化剂,具有较高的活性。
①该催化剂中铁元素的化合价为______。
②图1表示两种不同方法制得的催化剂CoxNi(1-x)Fe2O4在10℃时催化分解6%的H2O2溶液的相对初始速率随x变化曲线。由图中信息可知:______________法制取得到的催化剂活性更高;Co2+、Ni2+两种离子中催化效果更好的是______。
(2)草酸钴是制备钴的氧化物的重要原料。下图2为二水合草酸钴(CoC2O4·2H2O)在空气中受热的质量变化曲线,曲线中300℃及以上所得固体均为钴氧化物。
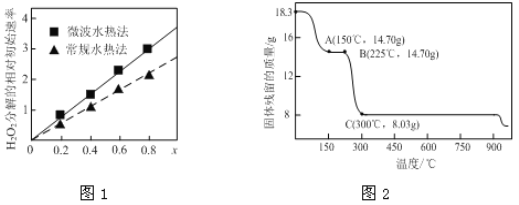
①通过计算确定A点剩余固体的化学成分为________________(填化学式)。试写出B点对应的物质与O2在225℃~300℃发生反应的化学方程式:_________________________________________。
②取一定质量的二水合草酸钴分解后的钴氧化物(其中Co的化合价为+2、+3),用480 mL 5 mol/L盐酸恰好完全溶解固体,得到CoCl2溶液和4.48 L(标准状况)黄绿色气体。试确定该钴氧化物中Co、O的物质的量之比为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.22.4LCO和CO2的混合气体中所含的碳原子数一定是NA
B.常温常压下,32gO2和32gO3所含氧原子数都是NA
C.48gO2所含的分子数为3NA
D.标准状况下36 g H2O中原子的数目为6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)研究有机物的方法有很多,常用的有①核磁共振氢谱②蒸馏③重结晶④萃取⑤红外光谱⑥过滤,其中用于分子结构确定的有____(填序号)。
(2)下列物质中,其核磁共振氢谱中只有一个吸收峰的是____(填字母)。
A.CH3CH3 B.CH3COOH
C.CH3COOCH3 D.CH3OCH3
(3)某含碳、氢、氧三种元素的有机物,经燃烧分析实验测定其碳的质量分数是64.86%,氢的质量分数是13.51%,则其实验式是________。如图是该有机物的质谱图,则其相对分子质量为______,分子式为________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K2FeO4是一种集氧化、吸附、絮凝、消毒、杀菌、除臭等功能于一体的绿色高效水处理剂,已成为多个领域不可短缺的物质之一,工业制备工艺如图所示,回答下列问题:

(1)在湿法制备Na2FeO4工艺中,请写出氯碱工业过程中用惰性电极电解饱和NaCl溶液的离子方程式:___;NaClO与FeCl3在碱性条件下制备Na2FeO4的反应中被氧化的原子与被还原的原子个数比为____;可循环使用的物质为___(任写一种)。
(2)电解法制备Na2FeO4工艺中,阳极材料为铁平板,在使用前要经过粗砂和细砂打磨抛光,其目的为____;钛合金材料作阴极,电解质溶液为NaOH溶液,请写出阳极电极反应式:____。
(3)干法制备Na2FeO4工艺是最早发现的制备工艺,请写出NaClO固体、Fe(NO3)3·9H2O晶体、NaOH固体在高温熔融的条件下制备Na2FeO4的化学方程式:_____。
(4)请写出由Na2FeO4制备K2FeO4的化学方程式:____;请说明该反应能发生的原因:____。
(5)粗K2FeO4提纯时用-5℃饱和KOH的原因____;K2FeO4是绿色水处理剂,能对水起到杀菌、消毒,又能起到净水的作用,其原因为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示的装置中,A是氯气发生装置,C、D 为气体净化装置(C中装有饱和食盐水;D 中装有浓硫酸),E 是硬质玻璃管装有细铁丝网,F为干燥的空广口瓶,烧杯G 中装有氢氧化钠溶液。

试回答:
(1)实验室制氯气的化学方程式:_______________________________;
(2)C装置的作用是________________;D 装置的作用是__________________;E中发生化学反应的方程式为:_____________________________。
(3)烧杯G 中装有氢氧化钠溶液的作用是___________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电渗析法淡化海水的原理如图所示。已知海水中含![]() 等离子,电极为惰性电极。下列叙述正确的是
等离子,电极为惰性电极。下列叙述正确的是
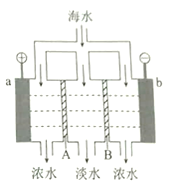
A. A是阳离子交换膜
B. 海水中阴离子移向b电极
C. a的电极反应为![]()
D. b极产生无色气体,出现白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题
(1)质子数为17、中子数为20的原子可表示为________,Na+的结构示意图________。
(2)焰色反应是_______变化,将碳酸钠进行焰色反应,火焰呈________。
(3)漂白粉有效成分的化学式________,漂白粉发挥漂白作用的反应方程式________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com