
【题目】醛类是香料中重要的一族,铃兰醛具有令人愉快的香味。以下是合称铃兰醛的一种路线:
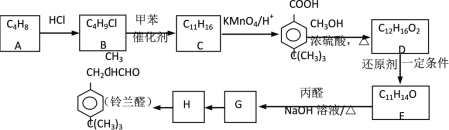
已知:① R1―CHO + R2―CH2―CHO ![]() R1―CH=C―CHO
R1―CH=C―CHO
② R―Cl +![]()
![]()
![]() + HCl
+ HCl
完成下列填空:
(1)写出A的名称_____________。
(2)写出结构简式:C_______;E_________。
(3)化合物M是G的芳香族同分异构体,M符合以下条件:
①能发生银镜反应;②在苯环的1,3,5位有三个侧链,其中两个烃基是C2H3和C4H9,则符合条件M的同分异构体共_______种。
(4)写出H生成铃兰醛的化学方程式:_______。
(5)E向G转化的过程中,常有分子式为C17H22O的副产物K产生。K的结构简式______。
【答案】2-甲基丙烯 ![]()
![]() 4 2
4 2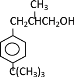 + O2
+ O2 ![]() 2
2 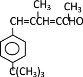 + 2H2O
+ 2H2O 
【解析】
由A、B的分子式判断A到B的反应是加成反应,由B、C的分子式可知,反应类似已知![]() 中取代反应反应,由C被酸性高锰酸钾溶液氧化的产物的结构,所以C的结构简式为
中取代反应反应,由C被酸性高锰酸钾溶液氧化的产物的结构,所以C的结构简式为 ,可推知A为
,可推知A为![]() ,B为
,B为![]() ,生成D的反应是酯化反应,则D的结构简式为
,生成D的反应是酯化反应,则D的结构简式为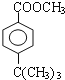 ,E到G发生类似已知
,E到G发生类似已知![]() 的反应,结合铃兰醛的结构,可知G的结构简式为
的反应,结合铃兰醛的结构,可知G的结构简式为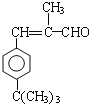 ,根据G的结构再比较D、E的分子式,判断E的结构简式为
,根据G的结构再比较D、E的分子式,判断E的结构简式为 ,G到铃兰醛的转化中碳碳双键被消除,则G与氢气发生加成反应生成H为
,G到铃兰醛的转化中碳碳双键被消除,则G与氢气发生加成反应生成H为 ,H再发生催化氧化生成铃兰醛;E向G转化的过程中,常伴有分子式为
,H再发生催化氧化生成铃兰醛;E向G转化的过程中,常伴有分子式为![]() 的副产物K产生,分子式可知,1分子F与丙醛得到的G后,G中醛基与丙醛继续进行
的副产物K产生,分子式可知,1分子F与丙醛得到的G后,G中醛基与丙醛继续进行![]() 中的反应生成K,据此回答。
中的反应生成K,据此回答。
![]() 为
为![]() ,A的名称为
,A的名称为![]() 甲基丙烯,故答案为:
甲基丙烯,故答案为:![]() 甲基丙烯;
甲基丙烯;
![]() 根据上面的分析可知,C的结构简式为
根据上面的分析可知,C的结构简式为 ;E的结构简式为
;E的结构简式为 ,故答案为:
,故答案为: ;
; ;
;
![]() 的结构简式为
的结构简式为 ,化合物M是G的芳香族同分异构体,M符合以下条件:
,化合物M是G的芳香族同分异构体,M符合以下条件:![]() 能发生银镜反应,说明有醛基;
能发生银镜反应,说明有醛基;![]() 在苯环的1,3,5位有三个侧链,其中两个烃基是
在苯环的1,3,5位有三个侧链,其中两个烃基是![]() 和
和![]() ,则符合条件的M的结构为苯环上连有三个侧链分别为
,则符合条件的M的结构为苯环上连有三个侧链分别为![]() 、
、![]() 、
、![]() ,其中
,其中![]() 、
、![]() 都只有一种结构,
都只有一种结构,![]() 有四种,故同分异构体共4种,故答案为:4;
有四种,故同分异构体共4种,故答案为:4;
![]() 为G加氢的产物,所以H生成生成铃兰醛发生醇的氧化反应,化学方程式为
为G加氢的产物,所以H生成生成铃兰醛发生醇的氧化反应,化学方程式为 ,故答案为:
,故答案为: ;
;
![]() 向G转化的过程中,常伴有分子式为
向G转化的过程中,常伴有分子式为![]() 的副产物K产生,因为G分子中仍存在醛基,可以与甲醛继续发生类似已知
的副产物K产生,因为G分子中仍存在醛基,可以与甲醛继续发生类似已知![]() 的反应,所以K的结构简式为
的反应,所以K的结构简式为 ,故答案为:
,故答案为: 。
。


科目:高中化学 来源: 题型:
【题目】扁桃酸衍生物是重要的医药中间体。以A和B为原料合成扁桃酸衍生物F的路线如下:
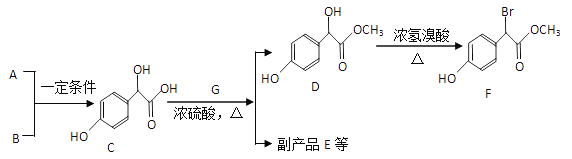
(1) A的分子式为C2H2O3,可发生银镜反应,且具有酸性,写出A+B→C的化学反应方程式:________
(2)C( )中①、②、③3个—OH的酸性由强到弱的顺序是______
)中①、②、③3个—OH的酸性由强到弱的顺序是______
(3)E是由2分子C生成的含有3个六元环的化合物,E分子中不同化学环境的氢原子有____种
(4)D→F的反应类型是________,1 mol F在一定条件下与足量NaOH溶液反应,最多消耗NaOH的物质的量为____mol,写出符合下列条件的F的同分异构体2种(不考虑立体异构)的结构简式:_____
①属于一元酸类化合物
②苯环上只有2个取代基且处于对位,其中一个是羟基
(5)已知:

A有多种合成方法,在方框中写出由乙酸合成A的路线流程图(其他原料任选) ______________(合成路线流程图示例如下:
H2C![]() CH2
CH2![]() CH3CH2OH
CH3CH2OH![]() CH3COOC2H5
CH3COOC2H5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全钒液流电池是一种新型的绿色环保储能电池。其电池总反应为:
![]() 。下列说法正确的是
。下列说法正确的是
A.放电时正极反应为:![]()
B.充电时阴极反应为:![]()
C.放电过程中电子由负极经外电路移向正极,再由正极经电解质溶液移向负极
D.充电过程中,H+由阴极区向阳极区迁移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH4和N2一定条件下能直接生成氨:3CH4(g)+2N2(g)![]() 3C(s)+4NH3(g)-Q,700℃时,CH4与N2在不同物质的量之比[n(CH4)/n(N2)]时CH4的平衡转化率如所示。正确的是
3C(s)+4NH3(g)-Q,700℃时,CH4与N2在不同物质的量之比[n(CH4)/n(N2)]时CH4的平衡转化率如所示。正确的是
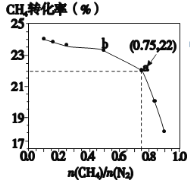
A.n(CH4)/n(N2)越大,CH4的转化率越高
B.n(CH4)/n(N2)不变时,升温,NH3的体积分数会增大
C.b点对应的平衡常数比a点的大
D.a点对应的NH3的体积分数约为13%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷有多种化合物,次磷酸(H3PO2)和次磷酸钠(NaH2PO2)常为化工生产中的还原剂。完成下列填空:
(1)H3PO2是一元中强酸,写出其电离方程式:_______;请将NaH2PO2溶液中的各离子按浓度由大到小的顺序排列:__________。
(2)室温下0.1mol/L的NaH2PO2溶液和0.1mol/L的Na2CO3溶液,pH更大的是_______,其原因是__________。
(3)化学镀银,可利用H3PO2把溶液中的Ag+还原为银的反应,已知该反应中还原剂与氧化剂的物质的量之比为1:4,则氧化产物是_______(填化学式)。
(4)工业上可用白磷(P4)与Ba(OH)2溶液反应生成PH3和Ba(H2PO2)2。写出并配平该反应的化学方程式________,若反应中转移电子6NA,用去还原剂_____mol。再向Ba(H2PO2)2溶液中加入盐酸制备H3PO2,有人说应该用硫酸代替盐酸,请说明用硫酸代替盐酸的优点:_______。
(5)下图是利用电解原理制备H3PO2的示意图(阳离子交换膜和阴离子交换膜分别只允许阳、阴离子通过;已知电极反应为:

阳极 4OH--4e→O2↑+ H2O
阴极 2H+ + 2e→H2↑):
分析在阳极室得到H3PO2原因:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是( )
A.石灰水中加入过量小苏打溶液:Ca2++OH-+HCO3-=CaCO3↓+H2O
B.用石墨作电极电解AlCl3溶液:2Cl-+2H2O![]() Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
C.酸性高锰酸钾溶液与H2O2溶液混合:2MnO4-+3H2O2+6H+=2Mn2++4O2↑+6H2O
D.0.2mol/L的NH4Al(SO4)2溶液与0.3mol/L的Ba(OH)2溶液等体积混合:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知AG=lg![]() ,电离度α=
,电离度α=![]() ×100%。常温下,向10mL0.1mol/LHX溶液中滴加0.1mol/LNaOH溶液,混合溶液中AG与滴加NaOH溶液体积的关系如图所示。
×100%。常温下,向10mL0.1mol/LHX溶液中滴加0.1mol/LNaOH溶液,混合溶液中AG与滴加NaOH溶液体积的关系如图所示。
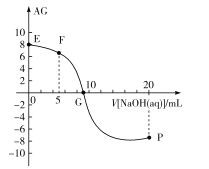
下列说法错误的是( )
A.F点溶液pH<7
B.G点溶液中c(Na+)=c(X-)>c(H+)=c(OH-)
C.V=10时,溶液中c(OH-)<c(HX)
D.常温下,HX的电离度约为1%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请阅读下列材料,完成下面小题。
随着社会经济的发展,汽车已进入千家万户,它给人们出行带来方便的同时汽车尾气污染问题也日益突显,汽车尾气中含NO、NO2、CO2、SO2和固体悬浮颗粒等。用活性炭还原处理氮氧化物是一种实用的氮氧化物转化方法:C(s)+2NO(g) ![]() N2(g)+CO2(g),可实现氮氧化物无害转化。
N2(g)+CO2(g),可实现氮氧化物无害转化。
【1】下列环境问题与汽车尾气的大量排放无关的是
A.酸雨B.温室效应C.PM2.5超标D.白色污染
【2】该反应属于化学基本反应类型中的
A.化合反应B.分解反应C.置换反应D.复分解反应
【3】该反应属于氧化还原反应,下列说法正确是
A.C元素被还原B.NO得到电子C.NO发生氧化反应D.CO2是氧化剂
【4】关于该反应下列说法不正确的是
A.升高温度能够加快反应速率
B.降低NO浓度能够减慢反应速率
C.使用合适的催化剂可以加快反应速率
D.加入足量的炭粉可以使NO 100%转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH=a的某电解质溶液中,插入两支惰性电极,通直流电一段时间后,溶液的pH>a,则该电解质可能是
A. Na2SO4 B. H2SO4 C. AgNO3 D. NaCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com