
【题目】ClO2是一种优良的消毒剂,熔点为-59.5℃,沸点为11.0℃,浓度过高时易发生分解引起爆炸,实验室在50℃时制备ClO2。
实验Ⅰ:制取并收集ClO2,装置如图所示:
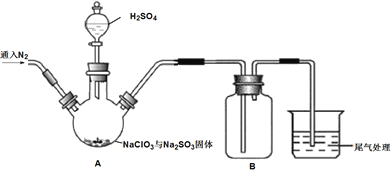
(1)写出用上述装置制取ClO2的化学反应方程式_____________。
(2)装置A中持续通入N2的目的是___________。装置B应添加__________(填“冰水浴”、“沸水浴”或“50℃的热水浴”)装置。
实验Ⅱ:测定装置A中ClO2的质量,设计装置如图:
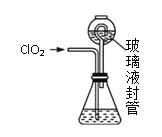
过程如下:
①在锥形瓶中加入足量的碘化钾,用100mL水溶解后,再加3mL硫酸溶液;
②按照右图组装好仪器;在玻璃液封管中加入①中溶液,浸没导管口;
③将生成的ClO2由导管通入锥形瓶的溶液中,充分吸收后,把玻璃液封管中的水封溶液倒入锥形瓶中,洗涤玻璃液封管2—3次,都倒入锥形瓶,再向锥形瓶中加入几滴淀粉溶液;
④用c mol·L1 Na2S2O3标准液滴定锥形瓶中的液体,共用去V mL Na2S2O3溶液(已知:I2+2S2O32-=2I+S4O62-)。
(3)装置中玻璃液封管的作用是_____________。
(4)滴定终点的现象是___________________。
(5)测得通入ClO2的质量m(ClO2)=_______g(用整理过的含c、V的代数式表示)。
【答案】![]() 降低ClO2的浓度,防止ClO2的浓度过高而发生分解,引起爆炸 冰水浴 防止ClO2逸出,使ClO2全部反应,准确测定ClO2的质量 溶液由蓝色变为无色,并且在30s内颜色不发生变化 1.35×10-2cV
降低ClO2的浓度,防止ClO2的浓度过高而发生分解,引起爆炸 冰水浴 防止ClO2逸出,使ClO2全部反应,准确测定ClO2的质量 溶液由蓝色变为无色,并且在30s内颜色不发生变化 1.35×10-2cV
【解析】
Ⅰ.(1)根据题给信息可知:NaClO3与亚硫酸钠在酸性条件下反应生成ClO2和硫酸钠等物质;
(2)二氧化氯(ClO2)沸点为11℃,NaClO3与亚硫酸钠在酸性条件下生成二氧化氯等物质, ClO2浓度过高时易发生分解引起爆炸,ClO2的沸点低,用冰水可以使ClO2冷凝为液体;
Ⅱ. (3)用水再次吸收残余的二氧化氯气体,并使锥形瓶内外压强相等,准确测量;
(4)溶液由蓝色恰好变为无色,且半分钟内不褪色,说明滴定至终点;
(5)根据氧化还原反应分析,有关系式2ClO2~5I2~10Na2S2O3计算n(ClO2),再根据m=nM计算m(ClO2)。
Ⅰ.(1)根据题给信息可知:NaClO3与亚硫酸钠在酸性条件下反应生成ClO2和硫酸钠等物质,则化学反应方程式为:![]() ,故答案为:
,故答案为:![]() ;
;
(2)二氧化氯(ClO2)沸点为11℃,NaClO3与亚硫酸钠在酸性条件下生成二氧化氯等物质, ClO2浓度过高时易发生分解引起爆炸,通入氮气,及时排出;ClO2的沸点低,用冰水可以使ClO2冷凝为液体,故答案为:降低ClO2的浓度,防止ClO2的浓度过高而发生分解,引起爆炸;冰水浴;
Ⅱ. (3)装置中玻璃液封管的作用是,防止ClO2逸出,使ClO2全部反应,准确测定ClO2的质量,故答案为:防止ClO2逸出,使ClO2全部反应,准确测定ClO2的质量;
(4)当滴入(最后)一滴标准液时,溶液由蓝色恰好变为无色,且半分钟内不褪色,说明滴定至终点,故答案为:溶液由蓝色变为无色,并且在30s内颜色不发生变化;
(5)VmLNa2S2O3溶液含有Na2S2O3物质的量n(Na2S2O3)=V10-3 L×cmol/L=cV10-3 mol.则:根据关系式: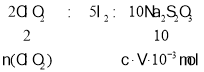 ,所以n(ClO2)=
,所以n(ClO2)=![]() n(Na2S2O3)=
n(Na2S2O3)=![]() ×cV10-3 mol,所以m(ClO2)=n(ClO2) M=
×cV10-3 mol,所以m(ClO2)=n(ClO2) M=![]() ×cV10-3 mol×67.5g/mol=1.35cV×10-2g,故答案为:1.35cV×10-2。
×cV10-3 mol×67.5g/mol=1.35cV×10-2g,故答案为:1.35cV×10-2。


 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案科目:高中化学 来源: 题型:
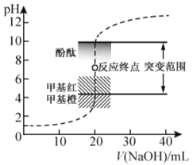
【题目】室温下,向![]() 盐酸中滴加
盐酸中滴加![]() 溶液,溶液的pH随
溶液,溶液的pH随![]() 溶液体积的变化如图。已知
溶液体积的变化如图。已知![]() 。下列说法不正确的是( )
。下列说法不正确的是( )
A.![]() 与盐酸恰好完全反应时,
与盐酸恰好完全反应时,![]()
B.选择变色范围在pH突变范围内的指示剂,可减小实验误差
C.选择甲基红指示反应终点,误差比甲基橙的大
D.![]() 时,
时,![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以SO2、软锰矿(主要成分为MnO2,少量Fe、Al、Ca及Pb的化合物等)、氨水及净化剂等为原料可制备MnSO4液和Mn3O4,主要实验步骤如下
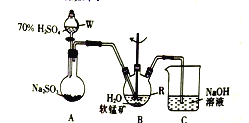
步骤I、如图所示装置,将SO2通入B中的软锰矿浆液中(MnO2+SO2=MnSO4)。
步骤II、充分反应后,在不断搅拌下依次向仪器R中加入适量纯净的MnO2、MnCO3,最后加入适量Na2S沉铅,
步骤III、过滤得MnSO4溶液
(1)仪器R的名称是_______。
(2)装置A用于制取SO2,反应的化学方程式为_________。
(3)装置B中的反应应控制在90~100℃,适宜的加热方式是______________。
(4)装置C的作用是______________________。
(5)“步骤Ⅱ”中加入纯净MnO2的目的是_______________,用MnCO3调节溶液pH时,需调节溶液pH的范围为________(该实验条件下,部分金属离子开始沉淀和沉淀完全的pH如下表)
金属离子 | Fe2+ | Fe3+ | Al3+ | Mn2+ |
开始沉淀的pH | 7.04 | 1.87 | 3.32 | 7.56 |
沉淀完全的pH | 9.18 | 3.27 | 4.9 | 10.2 |
(6)已知①用空气氧化Mn(OH)2浊液可制备Mn3O4[6Mn(OH)2+O2![]() 2Mn3O4+6H2O],主要副产物为MnOOH;反应温度和溶液pH对产品中Mn的质量分数的影响分别如图所示
2Mn3O4+6H2O],主要副产物为MnOOH;反应温度和溶液pH对产品中Mn的质量分数的影响分别如图所示

②反应温度超过80℃时,Mn3O4的产率开始降低,Mn(OH)2是白色沉淀,Mn3O4呈黑色;Mn3O4、MnOOH中锰的质量分数理论值依次为72.05%、62.5%请补充完整由步骤III得到MnSO4溶液,并用氨水等制备较纯净的Mn3O4的实验方案:______________________,真空干燥6小时得产品Mn3O4。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列卤代烃在KOH醇溶液中加热不发生消去反应的是( )
①![]() ②
② ③(CH3)3CCH2Cl ④CHCl2-CHBr2 ⑤
③(CH3)3CCH2Cl ④CHCl2-CHBr2 ⑤![]() ⑥CH3Cl
⑥CH3Cl
A.①③⑥B.②③⑤C.全部D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有以下几种有机物:
①![]() ②
②![]() ③
③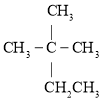 ④
④![]() ⑤
⑤![]()
⑥![]() ⑦
⑦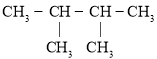 ⑧
⑧![]() ⑨
⑨![]()
请利用上述给出的物质按要求回答下列问题:
(1)③的系统命名是________。
(2)用“>”表示①③④⑧熔沸点高低顺序:________(填序号)。
(3)与③互为同系物的是________(填序号)。
(4)⑨的一氯代物同分异构体数目有________种。
(5)在120℃,![]() 条件下,某种气态烃与足量的
条件下,某种气态烃与足量的![]() 完全反应后,测得反应前后气体的体积没有发生改变,则该烃是________(填序号)。
完全反应后,测得反应前后气体的体积没有发生改变,则该烃是________(填序号)。
(6)写出⑥在铁作催化剂的条件下与液溴发生取代反应的化学方程式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按以下步骤可从![]() 合成
合成![]() (部分试剂和反应条件已略去)。
(部分试剂和反应条件已略去)。
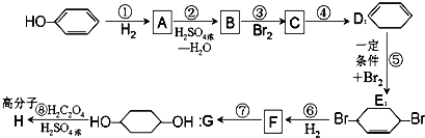
请回答下列问题:
(1)B,F的结构简式为:B___,F_______;
(2)反应①~⑦中属于消去反应的是(填代号)_______;
(3)根据反应![]() +Br2
+Br2![]()
![]() ,写出在同样条件下CH2=CHCH=CH2与等物质的量Br2发生加成反应的化学方程式:__;
,写出在同样条件下CH2=CHCH=CH2与等物质的量Br2发生加成反应的化学方程式:__;
(4)写出第④步C→![]() 的化学方程式(有机物写结构简式,注明反应条件)__;
的化学方程式(有机物写结构简式,注明反应条件)__;
(5)与4个不同的原子或原子团相连的碳原子称为手性碳原子;A﹣G这七种有机物分子中含有手性碳原子的是(填序号)__;
(6)核磁共振谱是测定有机物分子结构最有用的工具之一,在有机物分子中,不同位置的氢原子在质子核磁共振谱(PMR)中给出的峰值(信号)也不同,根据峰(信号)可以确定有机物分子中氢原子的种类和数目,例如:乙醛的结构式为:![]() ,其PMR谱中有2个信号峰,其强度之比为3:1,则下列有机物分子中,在质子核磁共振谱中能给出三种峰(信号)且强度之比为1:1:2的是__。
,其PMR谱中有2个信号峰,其强度之比为3:1,则下列有机物分子中,在质子核磁共振谱中能给出三种峰(信号)且强度之比为1:1:2的是__。
A ![]() B
B ![]() C
C ![]() D
D ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图装置中X和Y均为石墨电极,电解液为500mL某CuCl2溶液,电解时X电极表面有红色固体生成,Y电极有气体产生。一段时间后,取出X电极,洗涤、干燥、称量,电极增重1.6g。下列有关说法中正确的是
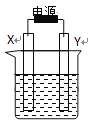
A. X电极连接电源正极
B. 生成气体体积为0.56L
C. Y电极上发生氧化反应
D. 该CuCl2溶液浓度为0.05mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常人们把拆开1 mol某化学键所消耗的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(△H),化学反应的△H等于反应物的总键能与生成物的总键能之差。
化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
键能/kJ·mol-1 | 46 | 360 | 436 | 431 | 176 | 347 |
工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)![]() Si(s)+4HCl(g),该反应的反应热△H为 ( )
Si(s)+4HCl(g),该反应的反应热△H为 ( )
A.+412 kJ·mol-1B.-412 kJ·mol-1
C.+236 kJ·mol-1D.-236 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸氢钾H2A的Ka1=1.1×103 ,Ka2=3.9×106)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。下列叙述错误的是

A. 混合溶液的导电能力与离子浓度和种类有关
B. Na+与A2的导电能力之和大于HA的
C. b点的混合溶液pH=7
D. c点的混合溶液中,c(Na+)>c(K+)>c(OH)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com