
分析 根据N=nNA可知,物质的量越大,其含有的分子数越多,先将各选项中的量转化成物质的量,然后进行比较即可.
解答 解:根据N=nNA可知,物质的量越大,其含有的分子数越多,
A..0.5molO2;
B.6.02×1023个N2的物质的量为1mol;
C.6.02×1024个HCl物质的量为:$\frac{6.02×1{0}^{24}}{6.02×1{0}^{23}}$=10mol;
D.0.12kg12C的物质的量为:$\frac{120g}{12g/mol}$=10mol,则与0.12kg12C含相同原子数目的Cl2的物质的量为:$\frac{10mol}{2}$=5mol;
根据分析可知,含有分子数由大到小的顺序为:C>D>B>A,
故答案为:C>D>B>A.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与阿伏伽德罗常数、摩尔质量之间的关系为解答关键,试题培养了学生的化学计算能力.


 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案科目:高中化学 来源: 题型:解答题

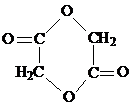 .
.


 (任写其中一种).
(任写其中一种).查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 将铜丝放在火焰上烧热,迅速插入乙醇中,可观察到铜丝表面由黑色变为红色,反复操作几次.还能闻到刺激性气味 | |
| B. | 向鸡蛋清溶液屮加入饱和硫酸铵溶液,有白色固体析出,再加入蒸馏水,振荡,固体又重新溶于水 | |
| C. | 向淀粉溶液中加入少量稀硫酸,加热4~5 min,待溶液冷却后,加入少量碘水,溶液呈蓝色,说明淀粉没有水解 | |
| D. | 取5mL0.1 mol•L-1 FeCl3,溶液,滴加0.1 mol•L1 KI溶液5~6滴,振荡,再加入少量KSCN溶液,溶液呈红色,说明该反应有一定的限度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向浓氨水中滴加饱和FeCl3溶液,可以制得Fe(OH)3胶体 | |
| B. | 为除去Mg(OH)2固体中少量Ca(OH)2,可用饱和MgCl2溶液多次洗涤后,再水洗、干燥 | |
| C. | 向溶液X中加入足量盐酸,产生无色无味气体,将气体通入澄清石灰水,产生白色沉淀,说明溶液X中含有CO32- | |
| D. | 验证炭与浓硫酸反应产生的CO2,将炭与浓硫酸反应生成的气体通入盛有澄清石灰水的试管中,观察是否有白色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 150 mL 1 mol/L盐酸 | B. | 20 mL 18.4 mol/L硫酸 | ||
| C. | 50 mL 3 mol/L盐酸 | D. | 250 mL 2 mol/L硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
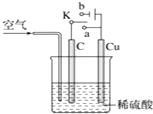 铜与稀硫酸不反应,某校实验小组的同学在老师的指导下设计了下列装置,实现了铜与稀硫酸的反应.请回答下列问题:
铜与稀硫酸不反应,某校实验小组的同学在老师的指导下设计了下列装置,实现了铜与稀硫酸的反应.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
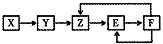 五种常见物质X、Y、Z、E、F均含有同一元素M,已知Y是单质,Z是NO(一氧化氮),在一定条件下它们有如下转化关系,下列推断不合理的是( )
五种常见物质X、Y、Z、E、F均含有同一元素M,已知Y是单质,Z是NO(一氧化氮),在一定条件下它们有如下转化关系,下列推断不合理的是( )| A. | X可能是一种氢化物 | B. | M不可能是金属 | ||
| C. | E可能是一种有色气体 | D. | X→Y一定是氧化还原反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com