
(11分)已知A、B、C、D、E是短周期中的五种非金属元素,它们的原子序数依次增大。A元素原子形成的离子核外电子数为零,C、D在元素周期表中处于相邻的位置,B原子的最外层电子数是内层电子数的2倍。E元素与D元素同主族;E的单质为黄色固体,易溶于二硫化碳。
(1)请写出元素符号: B___________、D___________。
(2)画出E的阴离子的结构示意图 ______________________。
(3)A的单质和C的单质在一定条件下反应生成化合物X,用电子式表示化合物X的形成过程:____________________________ _______。向X的水溶液中滴入酚酞溶液,会观察到什么现象:_________________________。
科目:高中化学 来源: 题型:
| A | B | C | D | |
| 分散到水中 | 得悬浊液 | 得无色溶液 | 液体分层,且下层为无色油状液体 | 得无色溶液 |
| 熔点(℃) | 1452 | -21.3 | -11.5 | 801 |
| 沸点(℃) | 1703 | 78.9 | 117 | 1210 |
查看答案和解析>>
科目:高中化学 来源: 题型:
请根据实验现象,按要求回答问题:
(1)将铁粉加入到C的溶液中,振荡过滤后,溶液的质量增加,颜色也有明显的变化。则可确认C中含有___________离子。发生反应的离子方程式为__________________________。
(2)用pH试纸测定,只有A、E两溶液呈碱性,且pH均为11。则A、E的化学式可能是_____________、_____________。为进一步确认A和E,现提供蒸馏水、pH试纸、量筒等实验用品,请你设计简单的实验方案:_______________________________________。
(3)将BaCl2溶液分别加入B和D的溶液中,只有D溶液中产生白色沉淀,且不溶于稀硝酸。则B、C、D的化学式分别是B_____________,C_____________,D_____________。
查看答案和解析>>
科目:高中化学 来源:2013届黑龙江省大庆实验中学高三上学期开学考试化学试卷(带解析) 题型:填空题
(11 分)已知 A、B、D为中学常见的单质,甲、乙、丙、丁、戊为短周期元素组成的化合物。其中,丙是一种能使湿润的红色石蕊试纸变蓝的无色气体;丁是一种高能燃料,其组成元素与丙相同,1 mol 丁分子中不同原子的数目比为1 :2,且含有18 mol电子;戊是一种难溶于水的白色胶状物质,既能与强酸反应,也能与强碱反应,具有净水作用。各物质间的转化关系如下图所示(某些条件已略去)。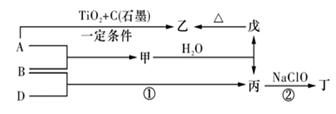
请回答:(1)单质B的组成元素在周期表中的位置是_________。
(2)戊的化学式为________。戊与强碱反应的离子方程式:________________
(3)丙中所包含的化学键类型有________ (填字母序号)。
a.离子键 b.极性共价键 c.非极性共价键
(4)反应①的化学方程式为________________________。
(5)反应②中,0.5mol NaClO参加反应时,转移1 mol电子,其化学方程式为_________
(6)—定条件下,A与TiO2、C(石墨)反应只生成乙和碳化钛(TiC),二者均为某些高温结构陶瓷的主要成分。已知,该反应生成1 mol乙时放出536 kJ热量,其热化学方程式为_______________________________。
查看答案和解析>>
科目:高中化学 来源:2010—20111学年河北省衡水中学高一上学期期末考试化学试卷 题型:填空题
(共 11 分)
(1)有一种叫做钾长石(K2Al2Si6O16),其化学式为写成氧化物的形式为______________
(2)反应3Cu+8HNO3 = 3Cu(NO3)2+2NO↑+4H2O 的离子方程式为:
每生成11.2L标准状况下的气体,被还原的 (填名称)的质量为 g。
得电子与失电子个数比是_____,被氧化与被还原的原子的个数比为______,试用“单线桥”标出该反应电子转移方向和数目:_____________________________ (3)已知A、B、C、D、E、F是含有同一种元素的化合物,其中F是能使红色湿润石蕊试纸变蓝的气体,它们之间能发生如下反应
(3)已知A、B、C、D、E、F是含有同一种元素的化合物,其中F是能使红色湿润石蕊试纸变蓝的气体,它们之间能发生如下反应
① A + H2O → B + C ② C + F → D ③ D + NaOH → F + E + H2O
写出A 、B、 C的化学式A______ B ____ C______
写出反应③的离子方程式
查看答案和解析>>
科目:高中化学 来源:2012-2013学年黑龙江省高三上学期开学考试化学试卷(解析版) 题型:填空题
(11 分)已知 A、B、D为中学常见的单质,甲、乙、丙、丁、戊为短周期元素组成的化合物。其中,丙是一种能使湿润的红色石蕊试纸变蓝的无色气体;丁是一种高能燃料,其组成元素与丙相同,1 mol 丁分子中不同原子的数目比为1 :2,且含有18 mol电子;戊是一种难溶于水的白色胶状物质,既能与强酸反应,也能与强碱反应,具有净水作用。各物质间的转化关系如下图所示(某些条件已略去)。

请回答:(1)单质B的组成元素在周期表中的位置是_________。
(2)戊的化学式为________。戊与强碱反应的离子方程式:________________
(3)丙中所包含的化学键类型有________ (填字母序号)。
a.离子键 b.极性共价键 c.非极性共价键
(4)反应①的化学方程式为________________________。
(5)反应②中,0.5mol NaClO参加反应时,转移1 mol电子,其化学方程式为_________
(6)—定条件下,A与TiO2、C(石墨)反应只生成乙和碳化钛(TiC),二者均为某些高温结构陶瓷的主要成分。已知,该反应生成1 mol乙时放出536 kJ热量,其热化学方程式为_______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com