
(1)某温度下体积为100 L的氨合成塔中(已知合成氨的反应为放热反应),测得各物质浓度(mol/L)的变化如下表:根据表中数据计算0 h~2 h内N2的平均反应速率 为 。请用下表中适当的数据表示该反应的平衡常数表达式: 。
| 时间/h | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| N2 | 1.500 | 1.400 | 1.200 | a | a | 0.900 | |
| H2 | 4.500 | 4.200 | 3.600 | b | b | 2.700 | 2.100 |
| NH3 | 0 | 0.200 | 0.600 | c | c | 0.200 | 0.600 |
(2)反应在4 h~5 h之间,平衡向正方向移动,可能的原因是
(选填A~F,下同)表中5h~6h之间数值发生变化,可能的原因是 。
A.移走了氨气 B.降低温度 C.加压
D.增加氢气浓度 E.升高温度 F.增加氮气浓度
(3)将NH3通入到0.04 mol·L-1的FeCl3溶液中,要使溶液中Fe3+
沉淀较完全(即Fe3+浓度降至原来的千分之一),则溶液的pH为
(已知常温下,Fe(OH)3的溶度积常数Ksp=4×10-38)
科目:高中化学 来源: 题型:阅读理解
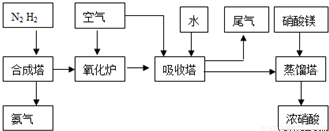
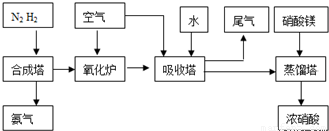
 (2009?中山模拟)工业合成氨与制备硝酸一般可连续生产,流程如下:
(2009?中山模拟)工业合成氨与制备硝酸一般可连续生产,流程如下: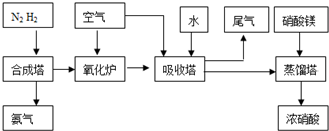
| 时间(h)浓度(mol/L) | 0 | 1 | 2 | 3 | 4 |
| N2 | 1.500 | 1.400 | 1.200 | C1 | C1 |
| H2 | 4.500 | 4.200 | 3.600 | C2 | C2 |
| NH3 | 0 | 0.200 | 0.600 | C3 | C3 |
| 1 |
| a |
| 1 |
| a |
查看答案和解析>>
科目:高中化学 来源: 题型:
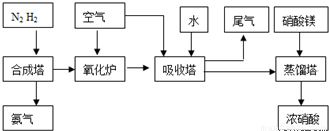
工业合成氨与制备硝酸一般可连续生产,流程如下:

(1)某温度下体积为200L的氨合成塔中,测得如下数据:
| 0 | 1 | 2 | 3 | 4 |
N2 | 1.500 | 1.400 | 1.200 | C1 | C1 |
H2 | 4.500 | 4.200 | 3.600 | C2 | C2 |
NH3 | 0 | 0.200 | 0.600 | C3 | C3 |
根据表中数据计算0~2小时内N2的平均反应速率 mol?L-1?h-1
若起始时与平衡时的压强之比为a,则N2的转化率为 (用含a的代数式表示)
(2)希腊阿里斯多德大学的 George Marnellos 和 Michael Stoukides,发明了一种合成氨的新方法,在常压下,把氢气和用氦气稀释的氮气分别通入一个加热到570℃的电解池,利用能通过氢离子的多孔陶瓷固体作电解质,氢气和氮气在电极上合成了氨,转化率达到78%,试写出电解池阴极的电极反应式
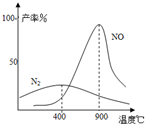
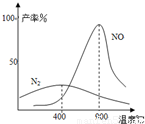
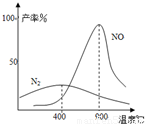
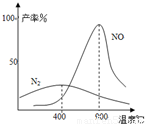
(3)氨气和氧气从145℃就开始反应,在不同温度和催化剂条件下生成不同产物(如右图):
 4NH3+5O2
4NH3+5O2![]() 4NO+6H2O K1=1×1053(900℃)
4NO+6H2O K1=1×1053(900℃)
4NH3+3O2![]() 2N2+6H2O K2=1×1067(900℃)
2N2+6H2O K2=1×1067(900℃)
![]() 温度较低时以生成 为主,温度高于900℃时,NO产率下降的原因 。吸收塔中需要补充空气的原因 。
温度较低时以生成 为主,温度高于900℃时,NO产率下降的原因 。吸收塔中需要补充空气的原因 。
![]() (4)尾气处理时小型化工厂常用尿素作为氮氧化物的吸收剂,此法运行费用低,吸收效果好,不产生二次污染,吸收后尾气中NOx的去除率高达99.95%。其主要的反应为氮氧化物混合气与水反应生成亚硝酸,亚硝酸再与尿素反应生成CO2 和N2请写出有关反应化学方程式 , 。
(4)尾气处理时小型化工厂常用尿素作为氮氧化物的吸收剂,此法运行费用低,吸收效果好,不产生二次污染,吸收后尾气中NOx的去除率高达99.95%。其主要的反应为氮氧化物混合气与水反应生成亚硝酸,亚硝酸再与尿素反应生成CO2 和N2请写出有关反应化学方程式 , 。
查看答案和解析>>
科目:高中化学 来源:2009年江苏省南通市通州区平潮高级中学高考化学模拟试卷(五)(解析版) 题型:填空题
| 时间(h)浓度(mol/L) | 1 | 2 | 3 | 4 | |
| N2 | 1.500 | 1.400 | 1.200 | C1 | C1 |
| H2 | 4.500 | 4.200 | 3.600 | C2 | C2 |
| NH3 | 0.200 | 0.600 | C3 | C3 |
查看答案和解析>>
科目:高中化学 来源:2011年江苏省徐州市睢宁县菁华学校高考化学一模试卷(解析版) 题型:填空题
| 时间(h)浓度(mol/L) | 1 | 2 | 3 | 4 | |
| N2 | 1.500 | 1.400 | 1.200 | C1 | C1 |
| H2 | 4.500 | 4.200 | 3.600 | C2 | C2 |
| NH3 | 0.200 | 0.600 | C3 | C3 |
查看答案和解析>>
科目:高中化学 来源:2009年广东省中山市高考化学模拟试卷(解析版) 题型:填空题
| 时间(h)浓度(mol/L) | 1 | 2 | 3 | 4 | |
| N2 | 1.500 | 1.400 | 1.200 | C1 | C1 |
| H2 | 4.500 | 4.200 | 3.600 | C2 | C2 |
| NH3 | 0.200 | 0.600 | C3 | C3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com