
| A. | 分子中3个碳原子在同一直线上 | |
| B. | 分子中所有原子都在同一平面上 | |
| C. | 分子中共价键的夹角为120° | |
| D. | 分子中共价键数为8,其中有一个碳碳双键 |
分析 乙烯是平面型结构,键角是120°,丙烯分子中也含有碳碳双键,所以丙烯分子中的3个碳原子在同一个平面内,但不在同一直线上;由于含有甲基,所以分子中所有原子不可能在同一平面,据此进行解答.
解答 解:A.丙烯分子中的3个碳原子在同一个平面内,但不在同一直线上,故A错误;
B.丙烯分子中含有甲基,所以分子中所有原子不可能在同一平面上,故B错误;
C.丙烯中甲基为立体结构,甲基中的碳氢键的夹角不是120°,故C错误;
D.丙烯分子中含有1个碳碳单键、1个碳碳双键和6个碳氢键,总共含有8个共价键,故D正确;
故选D.
点评 本题考查了有机物结构与性质,题目难度不大,明确乙烯、甲烷的结构为解答关键,注意熟练掌握常见有机物结构与性质,试题培养了学生的分析能力及知识迁移能力.


科目:高中化学 来源: 题型:选择题
| A. | 二氧化硫、二氧化氮、一氧化碳和二氧化碳是空气质量报告中涉及的主要污染物 | |
| B. | 正常雨水的pH等于7 | |
| C. | 二氧化硫和二氧化氮是引起酸雨的主要气体 | |
| D. | 家用汽车有利于人们出行,需要大力推广应用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Z的氢化物是同主族简单氢化物中最稳定的 | |
| B. | 非金属性:Z>Y>X | |
| C. | XY2中各原子最外层均满足8电子结构 | |
| D. | X、Y的最高价氧化物对应的水化物酸性后者强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
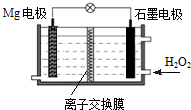 Mg-H2O2电池可用于无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如图.下列说法正确的是( )
Mg-H2O2电池可用于无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如图.下列说法正确的是( )| A. | Mg电极是该电池的正极 | B. | H2O2在石墨电极上发生氧化反应 | ||
| C. | 该电池的总反应为:Mg+H2O2═Mg(OH)2 | D. | 溶液中Cl-向正极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | H-Cl | Cl-Cl | H-H | C-H | C-Cl |
| 键能/(kJ•mol-1) | 431.4 | 242.1 | 435.9 | 413.0 | 338.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
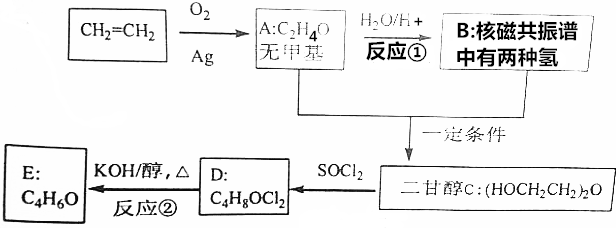
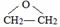 DClCH2CH2OCH2CH2Cl;
DClCH2CH2OCH2CH2Cl;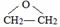 +H2O$\stackrel{H+}{→}$HOCH2CH2OH;反应②ClCH2CH2OCH2CH2Cl+2KOH$→_{△}^{醇}$CH2=CHOCH=CH2+2KCl+2H2O;
+H2O$\stackrel{H+}{→}$HOCH2CH2OH;反应②ClCH2CH2OCH2CH2Cl+2KOH$→_{△}^{醇}$CH2=CHOCH=CH2+2KCl+2H2O;查看答案和解析>>
科目:高中化学 来源:2016-2017学年重庆市高一上10月月考化学试卷(解析版) 题型:选择题
科学家己发现一种新型气态氢分子H3,在同温、同压下,等体积的H3和H2具有相同的
A.原子数 B.分子数 C.密度 D.质子数
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上第一次质检化学卷(解析版) 题型:填空题
A过滤法;B结晶法;C分液法;D萃取分液法;E蒸馏法;F升华法
(l)除去食盐水中的泥沙_________________(2)除去植物油中的水_________________
(3)将溶液中的硝酸钾与氯化钠分离____________(4)将自来水制为纯净水________________
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com