


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
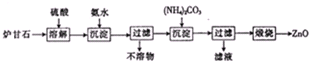
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、KOH溶液[K2CO3]:用Ca(OH)2溶液 |
| B、NaOH溶液[Ba(OH)2]:用Na2SO4溶液 |
| C、HNO3溶液[HCl]:用AgNO3溶液 |
| D、NaCl溶液[Na2SO4]:用Ba(NO3)2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等浓度的HCl和CH3COOH溶液中CH3COOH导电能力更弱 |
| B、常温时PH=3的CH3COOH溶液稀释100倍后PH<5 |
| C、某CH3COOH溶液中C(H+)很小 |
| D、CH3COONa溶液显碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素的非金属性:X>Y>Z |
| B、原子序数:X>Y>Z |
| C、气态氢化物的稳定性:XH3>YH3>ZH3 |
| D、气态氢化物的还原性:XH3<YH3<ZH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、a+b<c+d |
| B、平衡正向移动 |
| C、B的转化率降低 |
| D、C的体积分数降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、不慎将酸液溅到眼中,应立即用大量水冲洗,并一边眨眼 |
| B、不慎将碱液溅到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液 |
| C、洗去试管内壁附着的硫,可用二硫化碳 |
| D、配制硫酸溶液时,可先在量筒中加入一体积的水,再慢慢倒入浓硫酸,并不断搅拌 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、纯水在25℃和80℃时pH |
| B、25℃时,等体积的pH都等于3的盐酸和AlCl3的溶液中,已电离的水分子数 |
| C、25℃时,浓度均为0.1mol/L的FeCl3溶液和NH4Fe(SO4)2溶液中的c(Fe3+) |
| D、25℃时,中和体积与pH都相同的氢氧化钠溶液和氨水所消耗HCl的物质的量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com