
����Ŀ��(1)CaCO3��������Ϊ0.90��ʯ��ʯ100 kg��ȫ�ֽ����CO2________L����״����,ʯ��Ҥ�и�ʯ��ʯ100 kg�뽹̿���գ�����CO2 29120 L����״���������ʯ��ʯ��̼�����ȫ�ֽ⣬�ҽ�̿��ȫȼ�գ�������CO����̿������Ϊ__________g
(2)��25�桢101kPa�������£�ͬ������CH4�ͣ���������֮��Ϊ15��8����ص�Ħ��������_______________��
(3)������ͬ������ܱ�����X��Y����25���£�X�г���a gA���壬Y�г���a g CH4���壬X��Y�ڵ�ѹǿ֮����4��11����A��Ħ��������_______________��
���𰸡�20160 4800 30g/mol 44g/mol
��������
(1) n(CaCO3)=![]() ������CaCO3����CO2�����CaCO3��ȫ�ֽ����CO2�������n(CO2)=
������CaCO3����CO2�����CaCO3��ȫ�ֽ����CO2�������n(CO2)=![]() ��n(CaCO3)=900mol����̿ȼ������CO2���ʵ���Ϊ1300mol-900mol=400mol���Ӷ������̿��������
��n(CaCO3)=900mol����̿ȼ������CO2���ʵ���Ϊ1300mol-900mol=400mol���Ӷ������̿��������
(2)���ð����ӵ����ɵ����ۣ���������ʵ���֮�ȵ���������ȣ�����������ϵʽ���Ӷ����X��Ħ��������
(3)���ð����ӵ����ɵ����ۣ���������ʵ���֮�ȵ�����ѹǿ�ȣ�����������ϵʽ���Ӷ����A��Ħ��������
(1) n(CaCO3)=![]() ������CaCO3����CO2�����CaCO3��ȫ�ֽ����CO2�������V=900mol��22.4L/mol= 20160L��
������CaCO3����CO2�����CaCO3��ȫ�ֽ����CO2�������V=900mol��22.4L/mol= 20160L��
n(CO2)=![]() ��n(CaCO3)=900mol����̿ȼ������CO2���ʵ���Ϊ1300mol-900mol=400mol���Ӷ������̿������Ϊ400mol��12g/mol=4800g���ʴ�Ϊ��20160��4800��
��n(CaCO3)=900mol����̿ȼ������CO2���ʵ���Ϊ1300mol-900mol=400mol���Ӷ������̿������Ϊ400mol��12g/mol=4800g���ʴ�Ϊ��20160��4800��
(2)���ð����ӵ����ɵ����ۣ���������ʵ���֮�ȵ����������
�������������Ϊ1g��X��Ħ������ΪM
��![]() ���Ӷ����M=30g/mol���ʴ�Ϊ��30g/mol��
���Ӷ����M=30g/mol���ʴ�Ϊ��30g/mol��
(3)���ð����ӵ����ɵ����ۣ���������ʵ���֮�ȵ�����ѹǿ��
��A��Ħ������Ϊy
��![]() �����y=44g/mol���ʴ�Ϊ��44g/mol��
�����y=44g/mol���ʴ�Ϊ��44g/mol��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��0.1mol��CnHmCOOH����ʾ������ӳ�ʱ��50.8g�⣬0.1mol��������ȫȼ��ʱ������CO2��H2O��3.4mol���������ǣ�������
A. C15H27COOHB. C15H31COOH
C. C17H31COOHD. C17H33COOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������LiOH������������Ʊ�����ӵ���������ϡ����õ��LiCl��Һ�Ʊ�LiOH��װ����ͼ��ʾ������˵����ȷ����
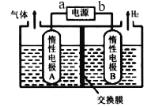
A.���Ե缫B������
B.��������Ϊa��A��B��b
C.�õ����õĽ���Ĥ�������ӽ���Ĥ
D.���������ĵ缫��Ӧ����ʽ��4OH- - 4e-=O2��+2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����0.2 L��NaCl��MgCl2��CaCl2��ɵĻ��Һ�У���������Ũ�ȴ�С��ͼ��ʾ���ش���������
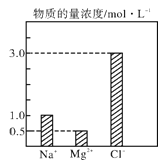
��1���û��Һ�У�NaCl�����ʵ���Ϊ_________mol��������MgCl2������Ϊ_______g��
��2���û��Һ��CaCl2�����ʵ���Ϊ___________mol�����û��Һ��ˮϡ�������Ϊ1 L��ϡ�ͺ���Һ��Ca2�������ʵ���Ũ��Ϊ__________mol��L��1��
��3�����ϡ�ͺ����Һ�м������������ữ����������Һ���ɵõ�����________mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ӦFeO(s)��CO(g) Fe(s)��CO2(g)��700 ��ʱƽ�ⳣ��Ϊ0.68��900��ʱƽ�ⳣ��Ϊ0.46������˵����ȷ����
A. �����¶ȸ÷�Ӧ������Ӧ���������淴Ӧ���ʼ�С
B. �÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪ��![]()
C. ����CO2Ũ�ȣ�ƽ�ⳣ������
D. �÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������һ�ֿ�ű��ҩ��о�������ҩ�������״����2019-nCOV�нϺ��������ã������Ǹ�ҩ��������୵ĺϳ�·�ߡ�
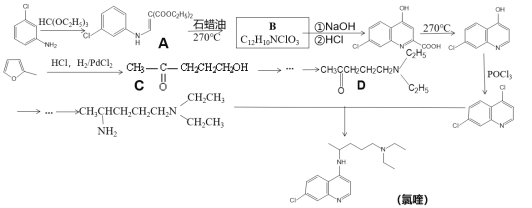
��֪����![]() ���з����ԣ�
���з����ԣ�
��R1-Cl+H2N-R2 �� R1-NH-R2+HCl
��ش�
��1������˵������ȷ����_________
A.����������� B.��୵ķ���ʽΪC18H24N3Cl
C.�����ϳɹ����а�����ȡ�����ӳɷ�Ӧ D.1molB����������3molNaOH
��2����д��Aת����B�Ļ�ѧ����ʽ_________
��3��Aת����B�Ĺ����л�������һ��˫��Ԫ���������ṹ��ʽΪ_________
��4����������ϩΪԭ�Ͻ��ϳ�·����C��D���ֲ�������������·ͼ��ʾ���������Լ���ѡ��_________
��5����д����������������![]() ��ͬ���칹��_________
��ͬ���칹��_________
��1HNMR����ʾ������ֻ��������H���ڷ�����ֻ����һ�����ṹ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȱ���ӻ�������ָ������������·��˹�ṹ��һ��ԭ��ͨ����������ʹ��۲�������ﵽ8��Hԭ�Ӵﵽ2���γɵ��ȶ����ӽṹ��Ҫ���һ��������˵���������
A.NH3��BF3��BF4-��ֻ��BF3��ȱ���ӻ�����
B.BF3��BF4-����ԭ�ӵ��ӻ���ʽ�ֱ�Ϊsp2��sp3
C.BF3��NH3��Ӧʱ����λ������
D.BF4-�ļ���С��NH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з��ӻ������У��۲���ӶԻ���ģ�ͣ����VSEPRģ�ͣ���VSEPRģ�ͼ��ι�������ӻ����ӵ����幹�Ͳ�һ�µ��ǣ�������
A. CO2B. H2OC. CO32��D. CCl4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�������ȷ�����Ǵ�ʵ�鰲ȫ�Ƕȿ��ǵ���
A.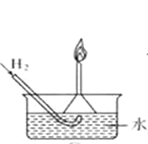 ʹ���Խ���Һ���µĵ���©�����������Ĵ���
ʹ���Խ���Һ���µĵ���©�����������Ĵ���
B.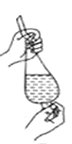 ʹ�� CCl4 ��ȡ��ˮ�е���ʱ���������ʹ©��������ų�
ʹ�� CCl4 ��ȡ��ˮ�е���ʱ���������ʹ©��������ų�
C.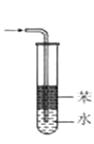 ���հ����Ȼ������岢��ֹ����
���հ����Ȼ������岢��ֹ����
D.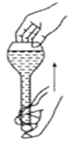 ��ʳָ��סƿ������һֻ����סƿ�ף���ƿ�������������ƿ�Ƿ�©ˮ
��ʳָ��סƿ������һֻ����סƿ�ף���ƿ�������������ƿ�Ƿ�©ˮ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com