【答案】
分析:A、依据溶液中氢离子浓度大小进行比较,:①CH
3COONa与NaHSO
4,溶液显酸性;②CH
3COONa与NaOH,溶液呈碱性;③CH
3COONa与NaCl,溶液中醋酸根离子水解显碱性;④CH
3COONa与NaHCO
3,醋酸根离子和碳酸氢根离子水解呈碱性;⑤CH
3COONa与NaHSO
3 醋酸根离子水解呈碱性,亚硫酸氢根离子电离大于水解显酸性;
B、①CH
3COONa与NaHSO
4,溶液显酸性;生成醋酸;②CH
3COONa与NaOH,溶液呈碱性;氢氧化钠溶液中氢氧根离子抑制醋酸根离子水解;③CH
3COONa与NaCl,溶液中醋酸根离子水解显碱性;④CH
3COONa与NaHCO
3,醋酸根离子和碳酸氢根离子水解呈碱性,相互抑制;⑤CH
3COONa与NaHSO
3 醋酸根离子水解呈碱性,亚硫酸氢根离子电离大于水解显酸性;促进醋酸根离子水解;
C、依据上述分析判断,c(CH
3COO
-)浓度大小为:②>⑤>③>④>①;
D、①CH
3COONa与NaHSO
4,溶液显酸性;生成醋酸;②CH
3COONa与NaOH,溶液呈碱性;氢氧化钠溶液中氢氧根离子抑制醋酸根离子水解;③CH
3COONa与NaCl,溶液中醋酸根离子水解显碱性;④CH
3COONa与NaHCO
3,醋酸根离子和碳酸氢根离子水解呈碱性,相互抑制;⑤CH
3COONa与NaHSO
3 醋酸根离子水解呈碱性,亚硫酸氢根离子电离大于水解显酸性;促进醋酸根离子水解.
解答:解:A、①CH
3COONa与NaHSO
4,溶液显酸性;②CH
3COONa与NaOH,溶液呈碱性;③CH
3COONa与NaCl,溶液中醋酸根离子水解显碱性;④CH
3COONa与NaHCO
3,醋酸根离子和碳酸氢根离子水解呈碱性;⑤CH
3COONa与NaHSO
3 醋酸根离子水解呈碱性,亚硫酸氢根离子电离大于水解显酸性;得到溶液中PH大小为:②>④>③>⑤>①,故A错误;
B、①CH
3COONa与NaHSO
4,溶液显酸性;生成醋酸;②CH
3COONa与NaOH,溶液呈碱性;氢氧化钠溶液中氢氧根离子抑制醋酸根离子水解;③CH
3COONa与NaCl,溶液中醋酸根离子水解显碱性;④CH
3COONa与NaHCO
3,醋酸根离子和碳酸氢根离子水解呈碱性,相互抑制;⑤CH
3COONa与NaHSO
3 醋酸根离子水解呈碱性,亚硫酸氢根离子电离大于水解显酸性;促进醋酸根离子水解;c(CH
3COOH)浓度为:①>⑤>③>④>②,故B错误;
C、依据上述分析判断,c(CH
3COO
-)浓度大小为:②>⑤>③>④>①,故C错误;
D、①CH
3COONa与NaHSO
4,溶液显酸性;生成醋酸;②CH
3COONa与NaOH,溶液呈碱性;氢氧化钠溶液中氢氧根离子抑制醋酸根离子水解;③CH
3COONa与NaCl,溶液中醋酸根离子水解显碱性;④CH
3COONa与NaHCO
3,醋酸根离子和碳酸氢根离子水解呈碱性,相互抑制;⑤CH
3COONa与NaHSO
3 醋酸根离子水解呈碱性,亚硫酸氢根离子电离大于水解显酸性;促进醋酸根离子水解;
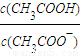
比值大小比较为::①>⑤>③>④>②,故D正确;
故选D.
点评:本题考查了电解质溶液中离子浓度大小比较,盐类水解应用,水解平衡,电离平衡的促进和抑制分析判断,题目难度较大.

 :②>③>④>⑤>①
:②>③>④>⑤>①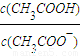 :①>⑤>③>④>②
:①>⑤>③>④>②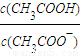 比值大小比较为::①>⑤>③>④>②,故D正确;
比值大小比较为::①>⑤>③>④>②,故D正确;

 科学实验活动册系列答案
科学实验活动册系列答案
 HCO3-+OH-HCO3-+H2O?H2CO3+OH-
HCO3-+OH-HCO3-+H2O?H2CO3+OH- HCO3-+OH-HCO3-+H2O?H2CO3+OH-
HCO3-+OH-HCO3-+H2O?H2CO3+OH-