
| c(Mn 2+) |
| C(Cu 2+) |
| C(Mn 2+)?C(S2-) |
| C(Cu2+)?C(S2-) |
| Ksp(MnS) |
| Ksp(CuS) |
| c(Mn 2+) |
| C(Cu 2+) |
| C(Mn 2+)?C(S2-) |
| C(Cu2+)?C(S2-) |
| Ksp(MnS) |
| Ksp(CuS) |


科目:高中化学 来源:2013-2014学年高考化学二轮专题冲刺第7讲 水溶液中的离子平衡练习卷(解析版) 题型:选择题
化工生产中含Cu2+的废水常用MnS(s)作沉淀剂,其反应原理为Cu2+(aq)+MnS(s)  CuS(s)+Mn2+(aq)。下列有关该反应的推理不正确的是(?? )
CuS(s)+Mn2+(aq)。下列有关该反应的推理不正确的是(?? )
A.该反应达到平衡时:c(Cu2+)=c(Mn2+)
B.CuS的溶解度比MnS的溶解度小
C.往平衡体系中加入少量Cu(NO3)2(s)后,c(Mn2+)变大
D.该反应平衡常数表达式:K=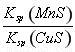
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com