
【题目】钇钡铜氧是一种新型节能高温超导体,其晶胞结构如图所示。研究发现,此高温超导体中的Cu元素有两种价态,分别为+2和+3,Y元素的化合价为+3,Ba元素的化合价为+2。

(1)该物质的化学式为________。
(2)该物质中Cu2+与Cu3+的个数比为__________。
【答案】YBa2Cu3O7 2:1
【解析】
(1)根据均摊法计算出晶胞中含有Y原子个数,再确定化学式;
(2)利用化合物中元素化合价代数和为零求得离子个数比。
(1)根据晶胞结构可知:Y在晶胞内,含有Y原子个数为1;Ba原子在晶胞内,含有Ba原子个数为2;Cu原子有位于晶胞顶点上的8个和位于侧棱上的8个,则晶胞中含有Cu原子个数为8×![]() +8×
+8×![]() =3;O原子有12个位于晶胞的棱上,8个位于侧面上,含有的O原子个数为12×
=3;O原子有12个位于晶胞的棱上,8个位于侧面上,含有的O原子个数为12×![]() +8×
+8×![]() =7,所以物质的化学式为YBaCu3O7;
=7,所以物质的化学式为YBaCu3O7;
(2)设该物质中+2价的Cu离子个数为x、+3价的Cu离子个数为y,根据化合物中元素化合价代数和为零可知:+3+2×2+2x+3y-2×7=0,且x+y=3,解得:x=2,y=1,所以+2价和+3价的Cu离子个数比为2:1。


科目:高中化学 来源: 题型:
【题目】金属镍及其化合物在合金材料以及催化剂等方面应用广泛。请回答下列问题:
(1)Ni原子的核外电子排布式为____________________;
(2)NiO、FeO的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69 pm和78 pm,则熔点NiO________FeO(填“<”或“>”);
(3)NiO晶胞中Ni和O的配位数分别为________、________;
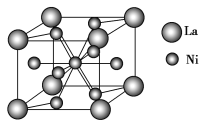
(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如图所示。该合金的化学式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组设计实验探究H2S的性质,装置如图所示。

下列说法正确的是( )
A. 若F中产生黑色沉淀,则说明H2SO4的酸性比H2S强
B. 若G中产生浅黄色沉淀,则说明H2S的还原性比Fe2+强
C. 若H中溶液变红色,则说明H2S是二元弱酸
D. 若E中FeS换成Na2S,该装置也可达到相同的目的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化硼(BN)晶体有多种结构。回答下列问题:
(1)六方氮化硼的结构与石墨相似(如图所示),具有层状结构,可作高温润滑剂,但不导电。该晶体中存在的作用力类型有___________,六方氮化硼晶体层内一个硼原子与相邻氮原子构成的空间构型为______________,六方氮化硼不导电的原因是__________。

![]()
(2)六方氮化硼在高温高压下,可以转化为立方氮化硼(如图所示),该晶胞边长为a pm,c原子的坐标参数为(0,0,0),e为(![]() ,
,![]() ,0),f为(
,0),f为(![]() ,0,
,0,![]() )。
)。
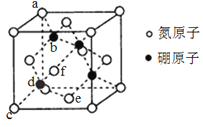
①由题干所给的坐标参数知,d原子的坐标参数为_________。
②B原子填充在N原子的四面体空隙,且占据此类空隙的比例为_________。
③a位置N原子与b位置B原子的距离为________pm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种元素位于元素周期表中前四周期,原子序数依次增大。A元素的价电子排布为nsnnpn+1;B元素原子最外层电子数是次外层电子数的3倍;C位于B的下一周期,是本周期最活泼的金属元素;D基态原子的3d原子轨道上的电子数是4s原子轨道上的4倍;E元素原子的4p轨道上有3个未成对电子。回答下列问题(用元素符号表示或按要求作答)。
(1)A、B、C的第一电离能由小到大的顺序为____________,三者电负性由大到小的顺序为_________。
(2)A和E的简单气态氢化物沸点高的是______,其原因是_________。
(3)D3+基态核外电子排布式为_________________。
(4)E基态原子的价电子轨道表示式为___________。
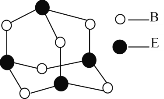
(5)B和E形成分子的结构如图所示,该分子的化学式为_______,E原子的杂化类型为________。
(6)B和C能形成离子化合物R,其晶胞结构如图所示:
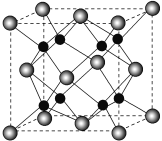
①一个晶胞中含______个B离子。R的化学式为__________。
②晶胞参数为a pm,则晶体R的密度为_____________gcm-3(只列计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用太阳能电解水制H2是解决能源危机的重要方向。采用固体氧化还原调节剂作为离子交换体系,实现H2、O2分离。下列分析正确的是( )
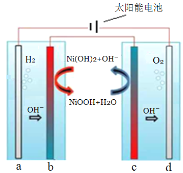
A.左侧电解池应选用酸性溶液,a极反应式为:2H+ + 2e-=H2↑
B.b极反应式:NiOOH + H2O + e-=Ni(OH)2 + OH-
C.c为阳极,发生氧化反应
D.电解一段时间后,可将b、c对调,循环利用物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在极性分子中,正电荷重心与负电荷重心间的距离称为偶极长,通常用![]() 表示。极性分子的极性强弱与偶极长和电荷量(
表示。极性分子的极性强弱与偶极长和电荷量(![]() )有关,一般用偶极矩(
)有关,一般用偶极矩(![]() )来衡量。分子的偶极矩是偶极长和电荷量的乘积,即
)来衡量。分子的偶极矩是偶极长和电荷量的乘积,即![]() 。在非极性分子中,其正、负电荷重心重合,故
。在非极性分子中,其正、负电荷重心重合,故![]() 为0。试回答下列问题:
为0。试回答下列问题:
(1)HCl、CS2、H2S、SO2四种分子中![]() 的有______________________________。
的有______________________________。
(2)实验测得:![]()
①由此可知,PF3分子的空间构型为____________________;
②BCl3分子的空间构型为____________________,中心原子的杂化方式为____________________。
(3)治癌药物![]() 具有平面四边形结构,Pt处在四边形中心,NH3和Cl分别处在四边形的4个顶点。已知该化合物有两种同分异构体,棕黄色化合物的
具有平面四边形结构,Pt处在四边形中心,NH3和Cl分别处在四边形的4个顶点。已知该化合物有两种同分异构体,棕黄色化合物的![]() ,淡黄色化合物的
,淡黄色化合物的![]() 。试写出两种同分异构体的结构简式:____________________(棕黄色)、____________________(淡黄色),在水中溶解度较大的是____________________(填结构简式)。
。试写出两种同分异构体的结构简式:____________________(棕黄色)、____________________(淡黄色),在水中溶解度较大的是____________________(填结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关晶体的叙述不正确的是( )
A.氯化钠和氯化铯晶体中,阴离子的配位数均为6
B.金刚石为空间网状结构,由碳原子以sp3杂化轨道形成共价键
C.金属钠的晶体采用体心立方堆积,每个晶胞含2个原子,配位数为8
D.干冰晶体中,每个CO2分子周围紧邻12个CO2分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄铜矿是工业炼铜的原料,含有的主要元素是硫、铁、铜,请回答下列问题。
(l)基态硫原子中核外电子有____种空间运动状态。Fe2+的电子排布式是 ___。
(2)液态SO2可发生白偶电离2SO2=SO2++SO32-,SO32-的空间构型是 ___,与SO2+互为等电子体的分子有____(填化学式,任写一种)。
(3)CuCl熔点为426℃,融化时几乎不导电,CuF的熔点为908℃,沸点1100℃,都是铜(I)的卤化物,熔沸点相差这么大的原因是 ___。
(4)乙硫醇(C2H5SH)是一种重要的合成中间体,分子中硫原子的杂化形式是____。乙硫醇的沸点比乙醇的沸点____(填“高”或“低”),原因是____。
(5)黄铜矿主要成分X的晶胞结构及晶胞参数如图所示,X的化学式是 ___,其密度为 ___g/cm3(阿伏加德罗常数的值用NA表示)。
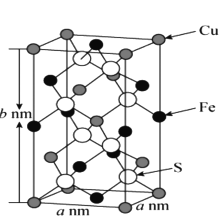
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com